题目内容
4.将饱和FeCl3溶液滴入沸水并煮沸一段时间,可得到红褐色液体.下列有关说法错误的是( )| A. | 光束通过该液体时形成光亮的“通路” | |
| B. | 插入石墨电极通直流电后,有一极附近液体颜色加深 | |
| C. | 向该液体中加入硝酸银溶液,无沉淀产生 | |
| D. | 将该液体加热、蒸干、灼烧后,有黑色固体生成 |
分析 将饱和FeCl3溶液滴入沸水并煮沸一段时间,可得到红褐色液体,该红褐色液体为氢氧化铁胶体,依据胶体具有丁达尔效应、电泳、聚沉的性质解答.
解答 解:将饱和FeCl3溶液滴入沸水并煮沸一段时间,可得到红褐色液体,该红褐色液体为氢氧化铁胶体.
A.胶体具有丁达尔效应,所以光束通过该液体时形成光亮的“通路”,故A正确;
B.胶体具有电泳性质,插入石墨电极通直流电后,有一极附近液体颜色加深,故B正确;
C.硝酸银为可溶性电解质,能够使氢氧化铁胶体产生聚沉而生成沉淀,且银离子能够与氯离子反应生成氯化银沉淀,故C错误;
D.将该液体加热、蒸干、灼烧后得到固体为氧化铁,氧化铁为红棕色固体,故D错误;
故选:CD.
点评 本题考查了胶体制备和性质,熟悉氢氧化铁胶体制备方法及胶体的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
15.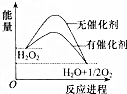 已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )
已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )
 已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )
已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图所示.下列说法正确的是( )| A. | 反应物的总能量高于生成物的总能量 | |
| B. | 加入催化剂,可提高H2O2的平衡转化率 | |
| C. | H2O2分解的热化学方程式:H2O2=H2O+O2;△H=-Q1 kJ•mol-1 | |
| D. | 加入催化剂,减小了反应的热效应 |
12.下列各组离子在溶液中能够大量共存的是( )
| A. | NH4+、NO3-、Na+、SO42- | B. | H+、Fe2+、Na+、NO3- | ||
| C. | Ba2+、K+、Al3+、HCO3- | D. | NH4+、Li+、OH-、SO42- |
19.反应3ClO-+2Fe3++10OH-═2FeO42-+5H2O+3Cl-,下列有关该反应的说法中正确的是( )
| A. | ClO-作氧化剂 | |
| B. | FeO42-为还原产物 | |
| C. | 每产生1 mol FeO42-,转移3 mol电子 | |
| D. | OH-作氧化剂 |
16.设NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为2NA | |
| B. | 7 g CnH2n中含有的氢原子数目为NA | |
| C. | 任何气体单质在标况下体积若为22.4L,则含有2NA个原子 | |
| D. | 1mol Na2O2与水反应转移的电子数约为1.204×1024个 |