题目内容
4.关于炔烃的描述中正确的是( )| A. | 分子组成符合CnH2n-2通式的链烃一定是炔烃 | |
| B. | 炔烃既易发生加成反应,又易发生取代反应 | |
| C. | 炔烃既能使溴水褪色,也能使酸性高锰酸钾溶液褪色 | |
| D. | 炔烃分子里所有的碳原子都在同一条直线上 |
分析 A.分子组成符合CnH2n-2的链烃,可能含有2个C=C双键,或1个C≡C三键;
B.炔烃难发生取代反应;
C.炔烃可以使高锰酸钾酸性溶液褪色;
D.炔烃中只有乙炔分子是直线型,其他炔烃分子的结构是多样的.
解答 解:A.分子组成符合CnH2n-2的链烃,可能含有2个C=C双键,为二烯烃,或1个C≡C三键,为炔烃,故A错误;
B.炔烃易发生加成反应难发生取代反应,故B错误;
C.炔烃既能使溴水褪色,也可以使高锰酸钾酸性溶液褪色,故C正确;
D.多碳原子的炔烃中碳原子不一定在一条直线上,如1-丁炔中的4个碳原子不在同一直线上,故D错误.
故选C.
点评 本题考查炔烃的性质,难度不大,注意根据炔烃中含有三键判断炔烃的性质.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
14.在蒸发皿中用酒精灯加热蒸干下列物质的溶液然后灼烧,可以得到该物质固体的是( )
| A. | 氯化铁 | B. | 碳酸氢钠 | C. | 硫酸铝 | D. | 高锰酸钾 |
15.设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 常温常压下,32克 O2与O3所含的原子数目相同,均为NA | |
| B. | 46克的NO2和N2O4混合气体中含原子数目为3 NA | |
| C. | 18克的NH4+中含有电子数为NA | |
| D. | 28 g Fe变为离子时,失去的电子数一定为NA |
12.下列有关说法正确的是( )
| A. | S(s,单斜)═S(s,正交)△H=+0.33kJ•mol?1,正交硫比单斜硫稳定 | |
| B. | 2H2(g)+O2(g)═2H2O(g);△H=-489.6kJ•mol-1,氢气的燃烧热为489.6kJ•mol-1 | |
| C. | 当镀锌铁制品的镀层破损时,镀层仍能对铁制品起到保护作用 | |
| D. | 锌锰干电池工作一段时间后碳棒变细 |
19.下列物质经催化加氢后能得到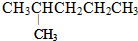 的是( )
的是( )
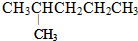 的是( )
的是( )| A. | CH3CH=CHCHCH2CH3 | B. | CH2=CHCHCH2CH3 | ||
| C. | CH≡CCHCH2CH3 | D. |  |
9.常温下,相同pH的硫酸溶液和硫酸铝溶液中由水电离出的c(H+)分别是1.0×10-amol/L和1.0×10-bmol/L,水的电离度分别是α1和α2,则下列关系正确的是( )
| A. | α1=α2 | B. | a+b=14 | C. | a<b | D. | a<7,b>7 |
16.如图为“铁链”图案,根据铁链上物质的分类依据,在M处应填入的物质是( )

| A. | CaCl2 | B. | Cl2O | C. | Cl2 | D. | NaClO3 |
13.检验溶液中的离子或物质,所用方法正确的是( )
| A. | 加入硝酸银溶液,有白色沉淀生成,证明一定有Cl-存在 | |
| B. | 加入BaCl2溶液和稀硝酸,有白色沉淀生成,证明一定有SO42- | |
| C. | 加入KSCN溶液和H2O2溶液,有血红色生成,证明一定含有Fe3+ | |
| D. | 加入KI淀粉溶液,变蓝色,说明可能有Cl2、Br2、I2 |