题目内容
E的产量是衡量一个国家石油化工发展水平的标志,并能进行如图所示的反应.
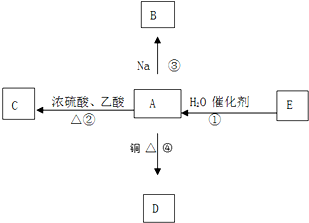
(1)写出A的官能团名称 ;
(2)下列反应的化学方程式
反应①: ,发生的反应类型 ;
反应②: ,发生的反应类型 ;
反应④: ,发生的反应类型 ;
(3)比较:反应①剧烈程度 (填>、=或<)钠和水反应的剧烈程度.

(1)写出A的官能团名称
(2)下列反应的化学方程式
反应①:
反应②:
反应④:
(3)比较:反应①剧烈程度
考点:有机物的推断
专题:有机物的化学性质及推断
分析:E的产量可衡量一个国家石油化工发展的水平,则E是乙烯(CH2=CH2),由框图中转化信息可知,E与水发生加成反应生成A为CH3CH2OH,A能与Na、乙酸反应,在红热铜丝发生催化氧化,结合框图中的转化关系、反应条件和反应试剂可推得,C是乙酸乙酯,D是乙醛,B是乙醇钠,然后结合有机物的结构与性质来解答.
解答:
解:E的产量可衡量一个国家石油化工发展的水平,则E是乙烯(CH2=CH2),由框图中转化信息可知,E与水发生加成反应生成A为CH3CH2OH,A能与Na、乙酸反应,在红热铜丝发生催化氧化,结合框图中的转化关系、反应条件和反应试剂可推得,C是乙酸乙酯,D是乙醛,B是乙醇钠,
(1)A为乙醇,官能团为羟基,故答案为:羟基;
(2)反应①为CH2=CH2+H2O→CH3CH2OH,属于加成反应;反应②为CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O,属于酯化反应;
反应④为2CH3CH2OH+O2
2CH3CHO+2H2O,属于氧化反应,
故答案为:CH2=CH2+H2O→CH3CH2OH;加成反应;CH3COOH+CH3CH2OH
CH3COOCH2CH3+H2O;酯化反应;2CH3CH2OH+O2
2CH3CHO+2H2O;氧化反应;
(3)水可电离出氢离子,而乙醇为中性物质,不能电离,则羟基H的活性为水>乙醇,则反应①剧烈程度<钠和水反应的剧烈程度,
故答案为:<.
(1)A为乙醇,官能团为羟基,故答案为:羟基;
(2)反应①为CH2=CH2+H2O→CH3CH2OH,属于加成反应;反应②为CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
反应④为2CH3CH2OH+O2
| Cu |
| △ |
故答案为:CH2=CH2+H2O→CH3CH2OH;加成反应;CH3COOH+CH3CH2OH
| 浓硫酸 |
| △ |
| Cu |
| △ |
(3)水可电离出氢离子,而乙醇为中性物质,不能电离,则羟基H的活性为水>乙醇,则反应①剧烈程度<钠和水反应的剧烈程度,
故答案为:<.
点评:本题考查有机物的成推断,涉及烯、醇、羧酸的性质与转化等,为高频考点,把握转化中官能团的变化、反应的条件为解答的关键,侧重常见有机物转化及性质的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列气体所含原子数最多的是( )
| A、0.5mol C2H6 |
| B、14g N2 |
| C、22g CO2 |
| D、32g O2 |
由CO、CO2和H2组成的混合气体在同温同压条件下与氮气的密度相同.则该气体中CO、CO2和H2的体积比为( )
| A、23:13:8 |
| B、13:29:8 |
| C、14:1:11 |
| D、16:57:26 |
下列物质之间的转化能够一步实现的是( )
| A、SiO2→H2SiO3 |
| B、Al2O3→Al(OH)3 |
| C、Fe→FeCl3 |
| D、S→SO3 |