题目内容
物质的量之比为2:5的锌与稀硝酸恰好反应,若硝酸被还原的产物为N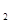 O,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是
O,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是
A.1:4 B.1:5 C.2:3 D.2:5
【答案】
A
【解析】
试题分析:设锌的物质的量是2x,则稀硝酸的物质的量是5x,因此生成硝酸锌的物质的量是2x,所以被还原的硝酸的物质的量是5x-4x=x。则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是x︰4x=1:4,答案选A。
考点:考查氧化还原反应的有关计算
点评:该题主要是考查学生利用守恒法解题的熟悉掌握程度,化学计算中最常用的方法就是各种守恒法,需要学生在平时的训练中注意总结和积累。

练习册系列答案
相关题目
物质的量之比为2:5的锌与稀硝酸反应,若硝酸被还原的产物为硝酸铵,反应结束后锌没有剩余,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是( )
| A、1:4 | B、2:3 | C、1:9 | D、2:5 |
将0.02mol铁粉加入0.05mol的FeCl3溶液中,充分反应后,其结果是( )
| A、铁有剩余 | B、往反应后溶液中滴入KSCN溶液不显红色 | C、Fe2+和Fe3+物质的量之比为6:1 | D、氧化产物与还原产物的物质的量之比为2:5 |