题目内容
1.25℃,pH=l的H2SO4溶液100mL,要使它变成pH=2的H2SO4溶液,可采用的方法为:(1)如果加入蒸馏水,应加入900mL;
(2)如果加入pH=3的H2SO4溶液,应加入1000mL.
(3)如果加入0.1mol/L的NaOH溶液,应加入$\frac{9}{110}$mL.
分析 (1)25℃,pH=l的H2SO4溶液100mL,要使它变成pH=2的H2SO4溶液,加水稀释10倍,最后溶液体积变化为1000ml;
(2)如果加入pH=3的H2SO4溶液,设需要溶液体积V,依据混合溶液PH计算;
(3)如果加入0.1mol/L的NaOH溶液,酸碱中和反应后剩余氢离子浓度为0.01mol/L,据此计算.
解答 解:(1)25℃,pH=l的H2SO4溶液100mL,要使它变成pH=2的H2SO4溶液,加水稀释10倍,最后溶液体积变化为1000ml,需要加入蒸馏水1000ml-100ml=900ml,
故答案为:900;
(2)如果加入pH=3的H2SO4溶液,设需要溶液体积V,
$\frac{0.1mol/L×0.1L+0.001mol/L×VL}{0.1L+VL}$=0.01mol/L,
V=1L=1000ml,故答案为:1000;
(3)如果加入0.1mol/L的NaOH溶液,酸碱中和反应后剩余氢离子浓度为0.01mol/L,c(H+)=$\frac{0.1mol/L×0.1L-0.1mol/L×V}{0.1L+VL}$=0.01mol/L,
V=$\frac{9}{110}$ml,故答案为:$\frac{9}{110}$.
点评 本题考查了溶液pH的计算,题目难度中等,注意掌握溶液酸碱性与溶液pH的计算方法,明确酸与酸、碱与碱、酸与碱的混合液的pH的计算方法,试题培养了学生的分析、理解能力及化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列说法或表示法错误的是( )
| A. | 化学反应过程中的能量变化除了热能外,还可以是光能、电能等 | |
| B. | 放热反应的△H<0 | |
| C. | 需要加热才能发生反应一定是吸热反应 | |
| D. | 反应物的总能量低于生成物的总能量时,发生吸热反应 |
12.观察下列几个装置示意图,有关叙述正确的是( )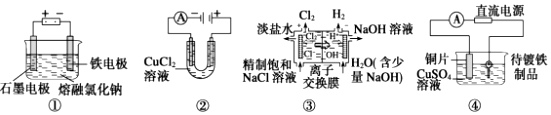

| A. | 装置①工业上可用于生产金属钠,电解过程中石墨电极产生金属 | |
| B. | 装置②中阳极产生的气体可以使湿润的淀粉碘化钾试纸变蓝 | |
| C. | 装置③中的离子交换膜允许阳离子、阴离子和小分子水通过 | |
| D. | 装置④的待镀铁制品应与电源正极相连 |
9.下列实验中,对应的现象以及结论都正确且两者具有因果关系是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 将稀硝酸加入过量铜粉中 | 溶液变蓝,试管口观察到了红棕色气体 | 铜将稀硝酸还原成二氧化氮 |
| B | 将SO2通入过量的饱和NaHCO3溶液中 | 有无色无味气体产生 | 非金属性:S大于C |
| C | 乙醇和浓硫酸混合加热,将产生的气体通入酸性高锰酸钾溶液中 | 酸性高锰酸钾溶液褪色 | 证明乙醇发生了消去反应产生烯烃 |
| D | 将0.1mol•L-1 MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol•L-1 CuSO4溶液 | 先有白色沉淀生成后变为浅蓝色沉淀 | Cu(OH)2的溶解度比Mg(OH)2的小 |
| A. | A | B. | B | C. | C | D. | D |
16.配制100mL 0.1000mol/L HCl溶液,下列有关配制实验的叙述正确的是( )
| A. | 所需仪器有:100mL容量瓶、烧杯、玻璃棒、胶头滴管、托盘天平 | |
| B. | 将量取的浓盐酸先倒入容量瓶,再加入蒸馏水至刻度线,摇匀 | |
| C. | 将溶液转移入容量瓶,要用玻璃棒引流 | |
| D. | 定容时俯视刻度,所配溶液浓度偏小 |
6.常温常压下,改变下列条件,能使饱和硫化氢溶液中$\frac{c({H}^{+})}{c({S}^{2-})}$增大的是( )
| A. | 通入少量NH3 | B. | 加入少量硫化钠 | C. | 通入少量Cl2 | D. | 通入少量H2S |
13.下列实验装置或操作设计正确、且能达到目的是( )

| A. | 实验I:实验室制备氨气 | |
| B. | 实验Ⅱ:用二氧化碳作喷泉实验 | |
| C. | 实验Ⅲ:进行中和热的测定 | |
| D. | 实验Ⅳ:电解氯化铜溶液得到铜和氯气 |
10.根据下列操作及现象,所得出的结论正确的是( )
| 序号 | 操作及现象 | 结论 |
| A | 将重晶石浸泡在饱和碳酸钠溶液中,一段时间后固体溶解 | Ksp(BaCO3)<Ksp(BaSO4) |
| B | 二氧化硫通入溴水中,溶液颜色褪去 | 二氧化硫具有漂白性 |
| C | 向NaOH和NaNO3的混合溶液中加入铝粉并加热,将湿润的红色石蕊试纸置于管口,试纸变蓝 | NO3-还原为NH3 |
| D | 将1.0mol•L-1Na2S溶液稀释到0.10mol•L-1,测得pH变小 | 稀释后S2-的水解程度减小 |
| A. | A | B. | B | C. | C | D. | D |
11.化学与生产、生活、科技等密切相关,下列说法正确的是( )
| A. | 由石油制取乙烯、丙烯等化工原料不涉及化学变化 | |
| B. | “神州七号”的防护层中含聚四氟乙烯,制备聚四氟乙烯的单体属于不饱和烃 | |
| C. | 浓硫酸可用于干燥SO2、C2H4、O2等气体 | |
| D. | 用CO2合成可降解的聚碳酸酯塑料,可以实现“碳”的循环利用 |