题目内容
室温下,下列叙述正确的是
A.pH=2的HA酸溶液与pH=12的MOH碱溶液以任意比混合:c(H+) + c(M+)=c(OH-) + c(A-)
B.对于0.1mol/LNa2SO3溶液:c(Na+)=2c(SO32-) + c(HSO3-) + 2c(H2SO3)
C.等浓度、等体枳的Na2CO3和NaHCO3混合: >
>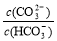
D.将足量AgCl分别放入:①5m水,②10mL0.2mol/LMgC12,③20mL0.3mol/L盐酸中溶解至饱和,c(Ag+):①>②>③
AC
【解析】
试题分析:A、根据电荷守恒可知:溶液中阳离子所带正电荷总数等于阴离子所带负电荷总数,所以pH=2的HA酸溶液与pH=12的MOH碱溶液以任意比混合:c(H+) + c(M+)=c(OH-) + c(A-),故A正确;B、根据物料守恒,对于0.1mol/LNa2SO3溶液:c(Na+)=2c(SO32-) + 2c(HSO3-) + 2c(H2SO3),故B错误;C、等浓度、等体枳的Na2CO3和NaHCO3混合: >1,
>1, <1,所以
<1,所以 >
> ,故C正确;D、②10mL0.2mol/LMgC12,Cl?浓度为0.4mol?L?1,③20mL0.3mol/L盐酸,Cl?浓度为0.3mol?L?1,溶解至饱和时c(Ag+):①>③>②,故D错误。
,故C正确;D、②10mL0.2mol/LMgC12,Cl?浓度为0.4mol?L?1,③20mL0.3mol/L盐酸,Cl?浓度为0.3mol?L?1,溶解至饱和时c(Ag+):①>③>②,故D错误。
考点:本题考查离子浓度比较。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 PCl3 (g)+Cl2(g)。达到平衡时,再向容器内通入一定量PCl5 (g),重新达到平衡后,与第一次平衡时相比,Cl2的浓度
PCl3 (g)+Cl2(g)。达到平衡时,再向容器内通入一定量PCl5 (g),重新达到平衡后,与第一次平衡时相比,Cl2的浓度