题目内容
等质量的两份锌粉a、b,分别加入过量的稀H2SO4中,同时向a中加入少量的CuSO4溶液,下图表示产生H2的体积(V)与时间(t)的关系,其中正确的是( )
D
解析试题分析:由于稀H2SO4是过量的,所以与Zn发生反应时放出的氢气按照Zn来计算。若其中的一份中加入少量的CuSO4溶液,就会发生反应:Zn+ CuSO4=ZnSO4+Cu.这样Zn、Cu及硫酸就形成了原电池,加快娿制取氢气的速率。但是由于消耗了一部分Zn,所以放出的氢气的量比不滴加要少一些。因此表示产生H2的体积(V)与时间(t)的关系正确的应该为D。
考点:考查原电池反应原理在实验室制取氢气的应用的知识。

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
将一定质量的镁和铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示。.则下列说法不正确的是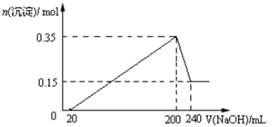
| A.镁和铝的总质量为9 g |
| B.最初20 mLNaOH溶液用于中和过量的硫酸 |
| C.硫酸的物质的量浓度为2.5 mol·L-1 |
| D.生成的氢气在标准状况下的体积为11.2 L |
NaCl是一种化工原料,可以制备一系列物质(如图所示)。下列说法正确的是 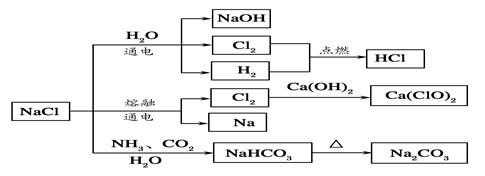
| A.25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| B.石灰乳和Cl2反应可制得漂白粉,其主要成分是次氯酸钙 |
| C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 |
| D.如图所示转化反应不都是氧化还原反应 |
下列关于碳酸钠和碳酸氢钠的说法不正确的是
| A.碳酸钠的热稳定性比碳酸氢钠强 |
| B.相同温度时,碳酸钠的溶解度大于碳酸氢钠 |
| C.同温度、同物质的量浓度时,碳酸钠溶液碱性大于碳酸氢钠溶液 |
| D.碳酸氢钠一定条件下可转化为碳酸钠,但碳酸钠不能转化为碳酸氢钠 |
下列现象或事实可用同一原理解释的是
| A.铁在冷的浓硫酸中和铝在冷的浓硝酸中都没有明显变化 |
| B.浓硫酸和浓盐酸长期暴露在空气中浓度降低 |
| C.SO2、漂白粉、活性炭、过氧化钠都能使红墨水褪色 |
| D.漂白粉和水玻璃长期暴露在空气中变质 |
为了验证小苏打中是否含有纯碱,下列实验操作及方法正确的是
| A.观察加热时是否放出气体 |
| B.观察滴加盐酸时能否放出气体 |
| C.溶于水中,再滴加石灰水,观察有无沉淀产生 |
| D.溶于水中,滴加少量的氯化钡溶液,观察有无白色沉淀产生 |
下列物质的转化在给定条件下能实现的是
①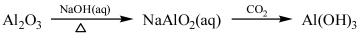
②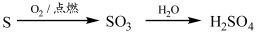
③
④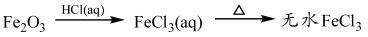
⑤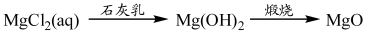
| A.①③⑤ | B.②③④ | C.②④⑤ | D.①④⑤ |
某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案: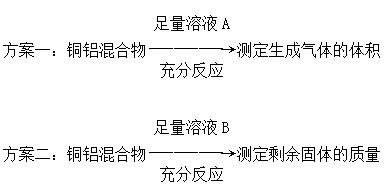
下列有关判断中不正确的是
| A.溶液A和溶液B均可以是盐酸或NaOH溶液 |
| B.若溶液B选用浓硝酸,测得铜的质量分数偏大 |
| C.方案一可能产生氢气,方案二可能剩余铜 |
| D.实验室中方案Ⅱ更便于实施 |
相同质量的下列物质分别与等浓度的NaOH溶液反应,至体系中均无固体物质,消耗碱量最多的是 ( )。
| A.Al | B.Al(OH)3 | C.AlCl3 | D.Al2O3 |