题目内容
20.已知氢氟酸、醋酸、氢氰酸(HCN)、碳酸在室温下的电离常数如下表,请回答下列问题:| ① | HF | Ka=6.8×10-4 mol•L-1 |
| ② | CH3COOH | Ka=1.7×10-5 mol•L-1 |
| ③ | HCN | Ka=6.2×10-10 mol•L-1 |
| ④ | H2CO3 | Ka1=4.4×10-7 mol•L-1 Ka2=4.7×10-11 mol•L-1 |
(2)写出H2CO3的电离方程式H2CO3?HCO3-+H+、HCO3-?CO32-+H+;
(3)写出化学方程式:足量的氢氟酸与碳酸钠溶液混合2HF+Na2CO3═2NaF+H2O+CO2↑足量的CO2通入NaCN溶液中NaCN+H2O+CO2═HCN+NaHCO3.
分析 (1)电离常数越大,电解质的酸性越强;
(2)碳酸为二元弱酸,分步电离,以第一步电离为主;
(3)酸性强弱HF>H2CO3>HCN,强酸可以制取弱酸,据此写出反应的化学方程式.
解答 解:(1)四种酸中HF的电离平衡常数最大,则HF酸最强,HCN的电离平衡常数最小,则HCN酸性最弱,
故答案为:HF;HCN;
(2)碳酸为二元弱酸,分步电离,以第一步电离为主,电离方程式为:H2CO3?HCO3-+H+、HCO3-?CO32-+H+,
故答案为:H2CO3?HCO3-+H+、HCO3-?CO32-+H+;
(3)酸性强弱HF>H2CO3>HCN>HCO3-,可发生反应生成NaF和CO2,反应的方程式为2HF+Na2CO3═2NaF+H2O+CO2↑,足量的CO2通入NaCN溶液中,发生的反应方程式为NaCN+H2O+CO2═HCN+NaHCO3,
故答案为:2HF+Na2CO3═2NaF+H2O+CO2↑;NaCN+H2O+CO2═HCN+NaHCO3.
点评 本题考查了弱电解质的电离,题目难度中等,明确弱电解质电离特点、电离平衡常数与酸的酸性强弱的关系是解本题关键,结合电离平衡的影响因素来分析解答,试题培养了学生的灵活应用能力.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
15.高温焙烧含硫废渣会产生SO2废气,为了回收利用SO2,研究人员研制了利用低品位软锰矿浆(主要成分是MnO2)吸收SO2,并制备硫酸锰晶体的生产流程,其流程示意图如下:

已知,浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子.有关金属离子形成氢氧化物沉淀时的pH见表:
请回答下列问题:
(1)高温焙烧:在实验室宜选择的主要仪器是坩埚.
(2)写出氧化过程中主要反应的离子方程式:2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,并调节溶液pH,pH应调节的范围是4.7≤pH<8.3.
(4)滤渣的主要成分有硫酸钙、氢氧化铁、氢氧化铝.
(5)工业生产中为了确定需要向浸出液中加入多少MnO2粉,可准确量取10.00mL浸出液用0.02mol/L酸性KMnO4溶液滴定,判断滴定终点的方法是当滴入最后一滴酸性KMnO4溶液,溶液变紫红色,且半分钟内不褪色.若达滴定终点共消耗10.00mL酸性KMnO4溶液,请计算浸出液中Fe2+浓度是0.1mol/L.

已知,浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子.有关金属离子形成氢氧化物沉淀时的pH见表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 7.6 | 9.7 |
| Fe3+ | 2.7 | 3.7 |
| Al3+ | 3.8 | 4.7 |
| Mn2+ | 8.3 | 9.8 |
(1)高温焙烧:在实验室宜选择的主要仪器是坩埚.
(2)写出氧化过程中主要反应的离子方程式:2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,并调节溶液pH,pH应调节的范围是4.7≤pH<8.3.
(4)滤渣的主要成分有硫酸钙、氢氧化铁、氢氧化铝.
(5)工业生产中为了确定需要向浸出液中加入多少MnO2粉,可准确量取10.00mL浸出液用0.02mol/L酸性KMnO4溶液滴定,判断滴定终点的方法是当滴入最后一滴酸性KMnO4溶液,溶液变紫红色,且半分钟内不褪色.若达滴定终点共消耗10.00mL酸性KMnO4溶液,请计算浸出液中Fe2+浓度是0.1mol/L.
12.在10mL 0.1mol•L-1氨水中逐滴加入0.1mol•L-1盐酸,当滴至混合液恰好呈中性时,消耗盐酸的体积( )
| A. | 等于10mL | B. | 小于10mL | C. | 大于10mL | D. | 等于5mL |
9.常温下,0.1mol•L-1的HA溶液中c(OH-)/c(H+)=1×10-8,下列叙述中正确的是( )
| A. | 0.01mol•L-1HA的溶液中c(H+)=1×10-4 mol•L-1 | |
| B. | PH=3的HA溶液与PH=11的NaOH溶液等体积混合后所得溶液中c(Na+)>c(A-)>c(OH-)>c(H+) | |
| C. | 浓度均为0.1 mol•L-1的HA溶液和NaA溶液等体积混合后所得溶液显酸性,则c(OH-)-c(H+)<c(HA)-c(A-) | |
| D. | PH=3的HA溶液与PH=11的NaOH溶液按体积比1:10混合后所得溶液中c(OH-)+c(A-)=c(H+)+c(Na+) |
 +H2O2
+H2O2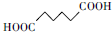 +H2O
+H2O

 ,其合成路线如图所示:
,其合成路线如图所示:
 .
. .
. .
.