题目内容
15.由IIIA 族元素A和VIA 族元素B组成的阴离子结构如下: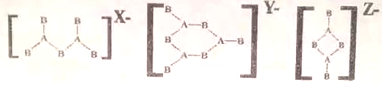
则所带电荷X、Y、Z依次为多少?( )
| A. | 4、4、2 | B. | 4、3、2 | C. | 3、3、2 | D. | 4、2、2 |
分析 A为IIIA 族元素,化合价为+3价,B为VIA 族元素元素,在形成的化合物中为-2价,结合化合价代数和为0计算电荷.
解答 解:A为IIIA 族元素,化合价为+3价,B为VIA 族元素元素,在形成的化合物中为-2价,由化合价代数和为0可知X=2×5-2×3=6,Y=2×6-3×3=3,Y=2×4-3×2=2,
故选B.
点评 本题考查原子结构与元素的性质,为高频考点,侧重考查学生的分析能力,本题注意根据元素所在主族确定化合价,结合化合价代数和为0的原子计算电荷,难度不大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案
相关题目
5.常温下有A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、盐酸和Na2SO4溶液中的一种.已知A、B溶液中水的电离程度相同,A、C溶液的pH相同.下列说法中不正确的是( )
| A. | D溶液的pH=7 | |
| B. | 四种溶液相比,C溶液中水的电离程度最大 | |
| C. | A与C等体积混合后,溶液中有c(Cl-)>c(H+)>c(NH4+)>c(OH-) | |
| D. | B与D等体积混合后,溶液中有c(OH-)=c(CH3COOH)+c(H+) |
10.NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,3.36L氧气与2.4g碳反应,生成CO2分子数为0.2NA | |
| B. | 标准状况下,1.12LCl2发生反应转移的电子数一定为0.1NA | |
| C. | lL0.lmol•L-1氨水中NH3•H2O分子数为0.1NA | |
| D. | 10g46%酒精(C2H5OH)中含氧原子总数大于0.1NA |
7.下列离子方程式正确的是( )
| A. | 向氯化铝溶液中加入过量氨水:A13++4NH3•H2O═AlO2-+2H2O+4NH4+ | |
| B. | 氧化铁溶于氢碘酸溶液中:Fe2O3+6H++2I-═2Fe2++I2+3H2O | |
| C. | 光导纤维在碱性环境中易断裂:Si+2OH-+H2O═SiO32-+2H2↑ | |
| D. | 澄清石灰水中加入过量小苏打溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O |
4.下列关于氯的说法中正确的是( )
| A. | Cl2具有很强的氧化性,在化学反应中只能作氧化剂 | |
| B. | Cl2和NaCl中均含有氯元素,它们的化学性质相同 | |
| C. | 实验室制备Cl2可用排饱和食盐水集气法收集 | |
| D. | 氯气、液氯和氯水是一种物质 |
5.VL硫酸钠中含Na+质量为m g,则溶液中SO42-的物质的量浓度为( )
| A. | $\frac{m}{23V}$mol/L | B. | $\frac{23}{mV}$mol/L | C. | $\frac{2m}{23V}$mol/L | D. | $\frac{m}{46V}$mol/L |