题目内容
4.下列关于氯的说法中正确的是( )| A. | Cl2具有很强的氧化性,在化学反应中只能作氧化剂 | |
| B. | Cl2和NaCl中均含有氯元素,它们的化学性质相同 | |
| C. | 实验室制备Cl2可用排饱和食盐水集气法收集 | |
| D. | 氯气、液氯和氯水是一种物质 |
分析 A、氯气在化学反应中既可以做氧化剂,还可以做还原剂;
B、Cl2和NaCl中均含有氯元素,但氯气具有强氧化性,而氯化钠中的氯是-1价最低价只能失电子;
C、氯气不溶于饱和食盐水;
D、氯气、液氯是纯净物,而氯水是混合物.
解答 解:A、氯气在和水以及强碱的反应中既做氧化剂,还做还原剂,故A错误;
B、Cl2和NaCl中均含有氯元素,但氯气具有强氧化性,而氯化钠中的氯是-1价最低价只能失电子,所以它们的化学性质不相同,故B错误;
C、氯气不溶于饱和食盐水,可用排饱和食盐水集气法收集,故C正确;
D、氯气、液氯是纯净物,而氯水是混合物,所以不是同一物质,故D错误;
故选C.
点评 本题考查物质的性质,为高频考点,把握物质的性质及发生的反应为解答的关键,侧重分析与应用能力的考查,注意把握氯气的性质,题目难度不大.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
14.一定温度下,在一容积不变的密闭容器中发生的可逆反应2X(g)?Y(g)+Z(s),不是反应达到平衡标志的是( )
| A. | 混合气体的压强不再变化 | B. | X、Y、Z的物质的量之比为2:1:1 | ||
| C. | 混合气体的密度不再变化 | D. | X的分解速率是Y的分解速率的两倍 |
15.由IIIA 族元素A和VIA 族元素B组成的阴离子结构如下:
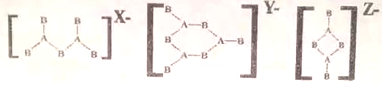
则所带电荷X、Y、Z依次为多少?( )

则所带电荷X、Y、Z依次为多少?( )
| A. | 4、4、2 | B. | 4、3、2 | C. | 3、3、2 | D. | 4、2、2 |
12.往CuO和铁粉的混合物中,加入一定量的稀H2SO4,并微热,当反应停止后,滤出不溶物,并向滤液中插入一枚铁钉,片刻后,取出铁钉,发现铁钉并无任何变化.根据上述现象,确定下面说法中正确的是( )
| A. | 不溶物一定是铜 | |
| B. | 不溶物一定是铁 | |
| C. | 不溶物中一定含铜,但不一定含铁 | |
| D. | 滤液中一定含有FeSO4,一定没有CuSO4 |
19. 一定条件下,体积为10L的密闭容器中,1molX和1mol Y进行反应:2X(g)+2Y(g)?Z(g),经60s达到平衡,生成0.3molZ.下列说法正确的是( )
一定条件下,体积为10L的密闭容器中,1molX和1mol Y进行反应:2X(g)+2Y(g)?Z(g),经60s达到平衡,生成0.3molZ.下列说法正确的是( )
 一定条件下,体积为10L的密闭容器中,1molX和1mol Y进行反应:2X(g)+2Y(g)?Z(g),经60s达到平衡,生成0.3molZ.下列说法正确的是( )
一定条件下,体积为10L的密闭容器中,1molX和1mol Y进行反应:2X(g)+2Y(g)?Z(g),经60s达到平衡,生成0.3molZ.下列说法正确的是( )| A. | 若升高温度,X的体积分数增大,则正反应的△H>0 | |
| B. | 将容器体积变为20L,Z的平衡浓度变为原来的$\frac{1}{2}$ | |
| C. | 以X浓度变化表示的反应速率为0.001mol/(L•s) | |
| D. | 若图纵坐标是正反应速率,则反应应该在绝热条件下进行,图象最高点为平衡点 |
9.在0.1mol•L-1氨水中加入少量的氯化铵晶体,则溶液的pH( )
| A. | 变小 | B. | 变大 | C. | 不变 | D. | 无法确定 |
16.下列实验的基本操作中,正确的是( )
| A. | 用同一个滴管取用不同的药品 | |
| B. | 将实验中剩余的药品放回原试剂瓶 | |
| C. | 实验前对实验装置进行气密性检查 | |
| D. | 将实验室制备的可燃性气体直接点燃 |
13.关于浓度均为0.1 mol/L的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是( )
| A. | 水电离出的c(H+):②>① | |
| B. | c(NH4+):③>① | |
| C. | ①和②等体积混合后的溶液:c(H+)=c(OH- )+c(NH3•H2O) | |
| D. | ①和③等体积混合后显碱性,c(NH4+)>c(Cl-)>c(NH3•H2O ) |
3.下列有关热化学方程式的叙述正确的是( )
| A. | 已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ/mol,则H2的燃烧热为-241.8 kJ/mol | |
| B. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应的热化学方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4 kJ/mol | |
| D. | 已知2SO2(g)+O2(g)?2SO3(g)△H=-QkJ•mol-1(Q>0),则将2mol SO2(g)和1mol O2(g)置于一密闭容器中充分反应后放出QkJ的热量 |