题目内容
下列反应方程式中,正确的是( )
| A、碳酸氢镁与足量的NaOH溶液反应:Mg2++2OH-═Mg(OH)2↓ |
| B、铝和过量的烧碱溶液反应:Al+2OH-═AlO2-+H2↑ |
| C、铝和稀硫酸溶液反应:Al+H+═Al3++H2↑ |
| D、氯化镁溶液与过量的氨水反应:Mg2++2NH3?H2O═Mg(OH)2↓+2NH4+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.漏掉碳酸氢根离子与氢氧根离子的反应;
B.原子个数不守恒;
C.电荷不守恒;
D.氯化镁溶液与过量的氨水反应,生成氢氧化镁和氯化铵.
B.原子个数不守恒;
C.电荷不守恒;
D.氯化镁溶液与过量的氨水反应,生成氢氧化镁和氯化铵.
解答:
解:A.碳酸氢镁与足量的NaOH溶液反应,离子方程式为:Mg2++2HCO3-+4OH-═Mg(OH)2↓+2CO32-+2H2O,故A错误;
B.铝和过量的烧碱溶液反应,离子方程式为:2Al+2H2O+2OH-═2AlO2-+3H2↑,故B错误;
C.铝和稀硫酸溶液反应,离子方程式为:2Al+6H+═2Al3++3H2↑,故C错误;
D.氯化镁溶液与过量的氨水反应,离子方程式为:Mg2++2NH3?H2O═Mg(OH)2↓+2NH4+,故D正确;
故选:D.
B.铝和过量的烧碱溶液反应,离子方程式为:2Al+2H2O+2OH-═2AlO2-+3H2↑,故B错误;
C.铝和稀硫酸溶液反应,离子方程式为:2Al+6H+═2Al3++3H2↑,故C错误;
D.氯化镁溶液与过量的氨水反应,离子方程式为:Mg2++2NH3?H2O═Mg(OH)2↓+2NH4+,故D正确;
故选:D.
点评:本题考查离子反应方程式的书写,明确物质之间反应的量的关系为解答的关键,注意离子反应的书写方法及化学式的拆分、电荷守恒.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案
相关题目
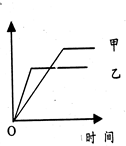 可用右侧示意图象表示的是( )
可用右侧示意图象表示的是( )| A、反应:等质量钾、钠分别与水反应,纵坐标:H 2质量,甲:钠,乙:钾 |
| B、反应:相同质量氨,在同一容器中2NH3?N2+3H2,纵坐标:氨气的转化率,甲:500℃,乙:400℃ |
| C、反应:体积比1:3的N2,H2,在体积可变的恒压容器中,2NH3?N2+3H2,纵坐标:氨气的浓度,甲:活性高的催化剂,乙:活性一般的催化剂 |
| D、反应:2mol S02与lmol 02,在相同温度下2S02+02?2S03,纵坐标:S03物质的量,甲:10atm,乙:2atm |
加入NaOH溶液,能使下列离子的浓度减小(不考虑溶液体积的变化)的是( )
| A、CO32- |
| B、AlO2- |
| C、SO32- |
| D、NH4+ |
玻璃棒是化学实验中常用的仪器,其作用是用于搅拌、过滤或转移液体时引流.下列有关实验过程中,肯定不需要使用玻璃棒进行的操作是( )
| A、一定溶质质量分数溶液的配制 |
| B、用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验 |
| C、用普通漏斗组成的过滤装置进行过滤实验 |
| D、将适量氯化铁饱和溶液滴入沸水中制氢氧化铁胶体 |
2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ?mol-1、CO(g)+
O2(g)=CO2(g)△H=-283kJ?mol-1某H2和CO的混合气体完全燃烧时放出113.74kJ热量,同时生成3.6g液态水,则原混合气体的H2和CO的物质的量之比( )
| 1 |
| 2 |
| A、2:1 | B、1:2 |
| C、1:1 | D、2:3 |
以下是一些食物的近似pH:(1)苹果3.3~4.5、(2)鸡蛋清7.6~8.0、(3)番茄4.0~4.4、(4)玉米粥6.8~8.0、(5)柑橘汁3.4~4.2,患胃痛、胃胀病的人宜经常食用的是( )
| A、(1)(4) |
| B、(4)(5) |
| C、(2)(4) |
| D、(3)(5) |
下列说法正确的是( )
| A、生铁的含碳量比钢要高,所以相同条件下钢比铁容易受到腐蚀 |
| B、灼烧某物质时,用眼直接观察到火焰呈黄色,则可以判断该物质不含钾元素 |
| C、向新制的FeSO4溶液中滴入适量的NaOH溶液,放置片刻,正个反应过程的颜色变化是:浅绿色溶液→白色沉淀→灰绿色沉淀→红褐色沉淀 |
| D、称取等质量的两份铝粉,分别加入过量稀HCl和过量的NaOH溶液.充分反应后,放出氢气的体积(同温同压下)前者小于后者 |
能正确表示下列反应的离子方程式是( )
| A、浓盐酸与铁屑反应:2Fe+6H+═2Fe3++3H2↑ |
| B、向CuSO4溶液中滴加过量氨水:2NH3?H2O+Cu2+═Cu(OH)2↓+2NH4+ |
| C、NaHCO3溶液与稀H2SO4反应:CO32-+2H+═H2O+CO2↑ |
| D、向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ |