题目内容
(12分)Fe2(SO4)3是一种重要的化工原料,完成下列问题:
(1)Fe2(SO4)3溶液中不能大量存在的粒子有 。
①Ag+ ②Cu2+ ③NO3- ④H+ ⑤Fe(OH)3胶体
(2)Fe2(SO4)3溶液和Ba(OH)2溶液反应的离子方程式为 。
(3)1LFe2(SO4)3溶液中,m(Fe3+)= a g ,则取出0.25L该溶液,c(SO42-)= 。
(4)①.某同学配制了0.05 mol·L-1的Fe2(SO4)3溶液,他用该Fe2(SO4)3溶液与12g 10%的NaOH溶液恰好完全反应,则该同学需取______ mLFe2(SO4)3溶液。
②.若该同学用新配制的Fe2(SO4)3溶液与含12g 10%的NaOH溶液恰好完全反应时,发现所需体积比①中所求的体积偏小,则可能的原因是___ ___。
A.配制溶液时,未洗涤烧杯
B.配制溶液时,未冷却至室温,立即配制完
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出
(1)①⑤(2)2Fe3++3SO42-+3Ba2++6OH-=2Fe(OH)3↓+3BaSO4↓(3) mol·L-1(无单位扣分)(4)①100 ② BC
mol·L-1(无单位扣分)(4)①100 ② BC
【解析】
试题分析:(1)Ag+和SO42- 会发生反应,不能大量存在,Cu2+ 、NO3- 、 H+不会发生反应,可以大量存在,溶液中不会大量存在Fe(OH)3胶体,故选①⑤。(2)Fe2(SO4)3溶液和Ba(OH)2溶液反应有两种沉淀生成,离子方程式为:2Fe3++3SO42-+3Ba2++6OH-=2Fe(OH)3↓+3BaSO4↓。(3)a g Fe3+的物质的量为:a/56mol,根据化学式中的个数知道SO42-的物质的量为3a/112mol, c(SO42-)=3a/112 mol÷1L=3a/112mol/L,溶液的浓度与体积无关,故 取出0.25L该溶液浓度还是3a/112 mol/L。
考点:离子共存问题、离子方程式的书写、有关物质的量的计算和溶液的配制。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
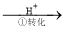 Cr2O72-
Cr2O72-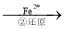 Cr3+
Cr3+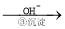 Cr(OH)3↓
Cr(OH)3↓ Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O 7H2O。
7H2O。