��Ŀ����
��ѡ����16�֣���ҵ��ˮ�г�����һ������Cr2O72����CrO42�������ǻ�����༰��̬ϵͳ�����ܴ���������д��������õĴ������������֡�
����1����ԭ������
�÷��Ĺ�������Ϊ��CrO42��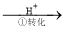 Cr2O72��
Cr2O72��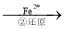 Cr3+
Cr3+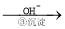 Cr(OH)3��
Cr(OH)3��
���еڢٲ�����ƽ�⣺2CrO42��(��ɫ)+2H��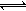 Cr2O72��(��ɫ)+H2O
Cr2O72��(��ɫ)+H2O
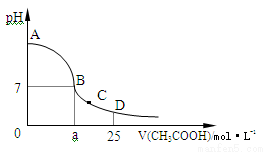
��1����ƽ����ϵ��pH=2������Һ�� ɫ��
��2����˵���ڢٲ���Ӧ��ƽ��״̬���� ��
A��Cr2O72����CrO42����Ũ����ͬ
B��2v (Cr2O72��)= v (CrO42��)
C����Һ����ɫ����
��3���ڢڲ��У���ԭ1molCr2O72�����ӣ���Ҫ mol��FeSO4 7H2O��
7H2O��
��4���ڢ۲����ɵ�Cr(OH)3����Һ�д��ڳ����ܽ�ƽ��,��д��������ܽ�ƽ�ⷽ��ʽ
�����£�Cr(OH)3���ܶȻ�Ksp=[Cr3+]��[OH?]3=10?32��Ҫʹc(Cr3+)����10?5mol/L����Һ��pHӦ���� ��
����2����ⷨ
�÷���Fe���缫��⺬Cr2O72�������Է�ˮ�����ŵ����У�������������ҺpH���ߣ�����Cr(OH)3������
��5����Fe���缫��ԭ���� ��
��������������ҺpH���ߵ�ԭ����(�õ缫��Ӧ����) ����Һ��ͬʱ���ɵij������� ��
(1)�� (2)c (3)6 (4) Cr(OH)3(s)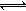 Cr3+(aq)+3OH?(aq) 5
Cr3+(aq)+3OH?(aq) 5
(5)������ӦΪFe��2e����Fe2+���ṩ��ԭ��Fe2+
��6)2H++2e����H2�� Fe(OH)3
��������
���������(1)pH=2����Һ�����ԣ������Գ�ɫ����2������ƽ���־��Ũ�Ȳ��䡢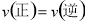 ������Һ����ɫ����ﵽƽ�⣻��3�����ݵ�ʧ�����غ㣬Cr��+6�۱�Ϊ+3�ۣ�1molCr2O72������Ҫ��6mol���ӣ�1mol��FeSO4
������Һ����ɫ����ﵽƽ�⣻��3�����ݵ�ʧ�����غ㣬Cr��+6�۱�Ϊ+3�ۣ�1molCr2O72������Ҫ��6mol���ӣ�1mol��FeSO4 7H2O ��ΪFe3+����ʧ����1mol��������Ҫ6mol FeSO4
7H2O ��ΪFe3+����ʧ����1mol��������Ҫ6mol FeSO4 7H2O����4��Cr(OH)3����Һ�г����ܽ�ƽ�ⷽ��ʽCr(OH)3(s)
7H2O����4��Cr(OH)3����Һ�г����ܽ�ƽ�ⷽ��ʽCr(OH)3(s)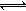 Cr3+(aq)+3OH?(aq) ��
Cr3+(aq)+3OH?(aq) ��
10?5��[OH?]3=10?32��[OH?]=10-9������PHӦΪ5����5��Fe������������������Ӧ������Fe2+��Fe2+��ԭCr2O72����������������ԭ��Ӧ��2H++2e����H2�������������ӣ�����PH����Fe2+������ΪFe3+���Ի�����Fe(OH)3������
���㣺���⿼��������ԭ�������ܽ�ƽ�⡢�绯ѧ��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�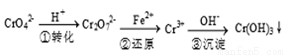
 Cr2O72-(��ɫ) +H2O
Cr2O72-(��ɫ) +H2O