题目内容
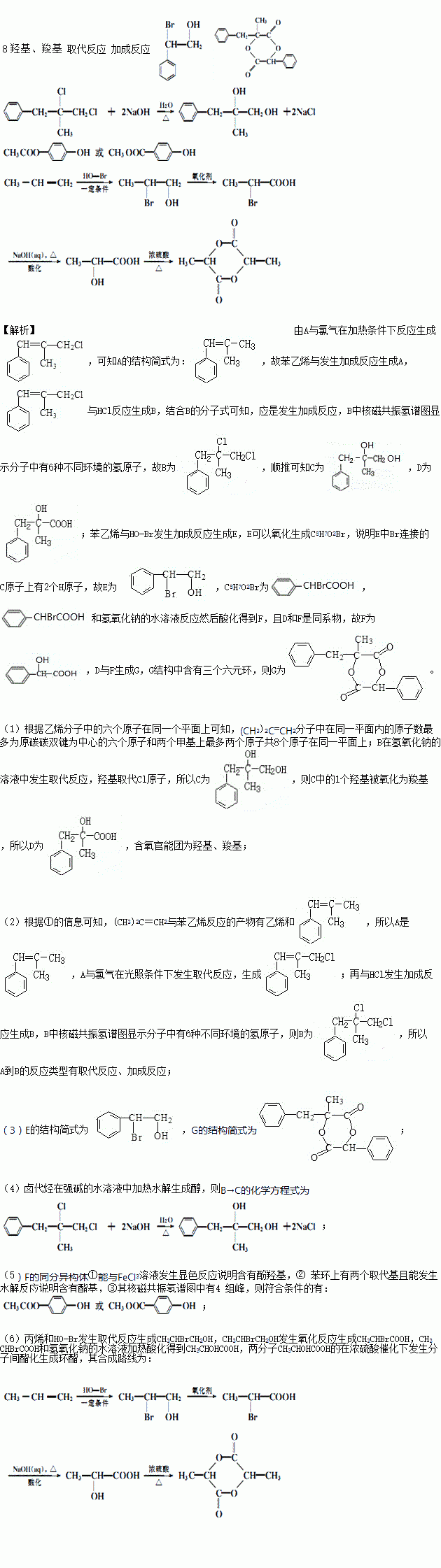
G是一种新型香料的主要成分之一,其结构中含有三个六元环。G的合成路线如下(部分产物和部分反应条件略去):

己知:① RCH=CH2+CH2=CHR?----CH2=CH2+RCH=CHR?;
② B的核磁共振氢谱图显示分子中有6 种不同环境的氢原子;
③D和F互为同系物。
(1)(CH3)2C=CH2,分子中在同一平面内的原子数最多为_____。D分子中含有的含氧官能团名称是________。
(2)A→B反应过程中涉及的反应类型依次为______、_______。
(3)E的结构简式为_______。G的结构简式为________。
(4)B→C的化学方程式为___________________。
(5)写出同时满足下列条件的F的一种同分异构体的结构简式__________。
①能与FeCl3溶液发生显色反应;② 苯环上有两个取代基且能发生水解反应;
③其核磁共振氢谱图中有4 组峰。
(6)模仿由苯乙烯合成F的方法,写出由丙烯制取 的合成路线:_______。
的合成路线:_______。
练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目

 CH3OH(g) △H1=-90.0 kJ• mol-1
CH3OH(g) △H1=-90.0 kJ• mol-1

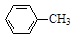 + 2KMnO4
+ 2KMnO4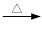
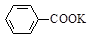 +KOH+2MnO2↓+H2O
+KOH+2MnO2↓+H2O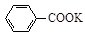 + HCl
+ HCl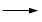
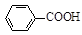 +KCl
+KCl
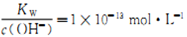 的溶液中:Na+、K+、AlO2-、NO3-
的溶液中:Na+、K+、AlO2-、NO3-