��Ŀ����
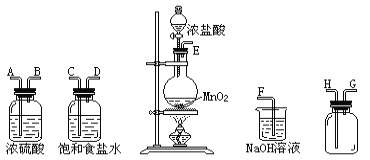
����Ŀ��ijУѧ������С���ͬѧ�����ͼ��ʾʵ��װ�ã�������֤һ����̼���л�ԭ�ԣ��ش��������⣺

(1)д��װ��A����������Ӧ�����ӷ���ʽ��__________��
(2)װ��B�������˵��Լ���_________________��
(3)��ʵ����û��װ��C��ʹװ��B��װ��Dֱ�����������ʵ����ɵ�Ӱ����_______��
(4)����ʵ���е�___________________����֤��CO���л�ԭ����
(5)��Ҫ����װ��F�г���ʯ��ˮ����ǵ�����ȷ��һ����̼���л�ԭ�ԣ�Ӧ����ͼװ��________��______֮��������ͼ�е�________װ��(�����)��

���𰸡�CaCO3+2H��=Ca2��+H2O+CO2�� ����̼��������Һ û�г�ȥ�����е�ˮ������������ˮ������̿��Ӧ����H2��CO��H2Ҳ�ܻ�ԭCuO��Ӱ��ʵ���� Eװ���к�ɫCuO��ɺ�ɫ D E ��
��������
��װ��A�������ʯ��ʯ��Ӧ���ɶ�����̼����Ӧ�����Ķ�����̼����ͨ��ʢ�е�NaHCO3������Һװ��B�п��Գ�ȥ���л��е�����HCl���壬������ͨ��Cװ���е�Ũ�������õ�����CO2����D�и��������£�C��CO2��Ӧ����CO��CO�ܻ�ԭCuO��������Cu��CO2��ʹ�����ɺ�ɫ��Ϊ��ɫ��CO2�ܹ�ʹ����ʯ��ˮ����ǡ���C��CO2��Ӧ�ķ�Ӧ�У�CO2��������ȫת��ΪCO�����Դ�Dװ�ó����������к���CO2��Ϊ��ֹδ��Ӧ��CO2�ĸ��ţ�Ӧ�Ȱ�ԭ����CO2��ȥ��
(1)װ��A�У������ʯ��ʯ��Ӧ���ɶ�����̼���Ȼ��ƺ�ˮ���䷴Ӧ���ӷ���ʽΪ��CaCO3+2H��=Ca2��+H2O+CO2����
(2)ʵ�����������ʯ��ʯ��ȡCO2���÷�Ӧ�Ƿ��ȷ�Ӧ����Ӧ�ų����������������е�HCl�ӷ��������ȡ��CO2�к�������HCl���壬Ϊ��ȥHCl���壬ͬʱ������CO2���壬ѡȡ���Լ�Ӧ�ܳ�ȥ�Ȼ��������Ҳ��Ͷ�����̼��Ӧ��һ�㳣�ñ��͵�NaHCO3��Һ��
(3)װ��C�������Ǹ���CO2���壬��û�и�װ�ã�CO2�е�ˮ����������Ҳ������C��Ӧ����H2��CO��H2Ҳ�ܻ�ԭCuO��������CO���л�ԭ�ԣ�
(4)�ڸ��������£���װ��D��CO2��C��Ӧ����CO������Dװ���еĺ�ɫ������̿����Ӧ����ʽΪCO2+C![]() 2CO��һ����̼���л�ԭ�ԣ���װ��E�з�����Ӧ��CO+CuO
2CO��һ����̼���л�ԭ�ԣ���װ��E�з�����Ӧ��CO+CuO![]() Cu+CO2������CO�ܻ�ԭ��ɫ������ͭ��ʹ���Ϊ��ɫ��ͭ���ʣ����Eװ���к�ɫCuO��ɺ�ɫ����֤����CO�Ļ�ԭ�ԣ�
Cu+CO2������CO�ܻ�ԭ��ɫ������ͭ��ʹ���Ϊ��ɫ��ͭ���ʣ����Eװ���к�ɫCuO��ɺ�ɫ����֤����CO�Ļ�ԭ�ԣ�
(5)�ڸ��������£�C��CO2��Ӧ����CO��CO2��������ȫת��ΪCO��������Dװ�ó����������к���CO2��Ϊ��ֹδ��Ӧ��CO2�ĸ��ţ�Ӧ�Ȱ�D������CO2��ȥ���ٽ�CO����ͨ��Eװ�á�������D��E֮������һ�� ��ȥCO2��װ�ã�����CO2����������������ü��Թ������ʳ�ȥ�����ʵ�װ���Ǣڡ�