题目内容
14.下列物质中,不能用玻璃瓶来盛装的是( )| A. | 烧碱溶液 | B. | 浓硫酸 | C. | 氢氟酸 | D. | 碳酸钠溶液 |
分析 玻璃中含有二氧化硅,二氧化硅是酸性氧化物,能和氢氟酸、强碱溶液反应,以此解答该题.
解答 解:A.二氧化硅和氢氧化钠溶液生成粘性的硅酸钠,但玻璃瓶内壁光滑,导致二氧化硅和氢氧化钠不易反应,所以可以用玻璃瓶盛放,故A正确;
B.浓硫酸与二氧化硅不反应,可用玻璃瓶盛放,故B正确;
C.氢氟酸和二氧化硅反应生成四氟化硅而腐蚀玻璃,所以不能用玻璃瓶盛,故C错误;
D.碳酸钠溶液碱性较弱与二氧化硅不反应,可用玻璃瓶盛放,故D正确.
故选C.
点评 本题以化学试剂的存放为载体考查了二氧化硅的性质,注意二氧化硅是酸性氧化物,和强酸不反应,但能和氢氟酸反应,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.下列实验操作、现象或结论正确的是( )
| A. | 蒸发操作时,应使蒸发皿中的水分完全蒸干后,才能停止加热 | |
| B. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| C. | 除去铜粉中混有的少量镁粉和铝粉可加入足量氢氧化钠溶液,反应后过滤、洗涤 | |
| D. | 加入盐酸,放出无色气体,该气体能使澄清石灰水变浑浊的气体,则原溶液中有CO32- |
2.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 通常状况下,2.24 L NO2和N2O4的混合气体中氮原子和氧原子数比为1:2 | |
| B. | 标准状况下,22.4 L己烷中共价键数目为19NA | |
| C. | 1 mol/L的Na2CO3溶液中所含阴离子数大于NA个 | |
| D. | 100 mL 0.3 mol/L 的硝酸溶液和200 mL 0.25 mol/L 的硫酸溶液混合配制成500 mL 混合溶液,则该溶液中的氢离子浓度为0.55 mol/L |
19.下列化学实验事实及其解释都正确的是( )
| A. | 氯气可以使湿润的有色布条褪色,是因为氯气分子能漂白有机分子 | |
| B. | SO2溶于水,其水溶液能导电,说明SO2是电解质 | |
| C. | 用饱和Na2CO3溶液可将BaSO4转化为BaCO3,说明Ksp(BaSO4)>Ksp(BaCO3) | |
| D. | 某溶液用盐酸酸化无明显现象,再滴加氯化钡溶液有白色沉淀,说明溶液中有SO42- |
6.下列物质按纯净物、混合物、强电解质、弱电解质、非电解质的顺序组合的是( )
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 盐酸 | 水煤气 | 硫酸 | 醋酸 | HD |
| B | 胆矾 | 石灰水 | 硫酸钡 | HNO2 | NH3 |
| C | 火碱 | 蔗糖溶液 | 氯化钠 | 氨水 | 三氧化硫 |
| D | 冰醋酸 | 福尔马林 | 苛性钾 | 碘化氢 | 乙醇 |
| A. | A | B. | B | C. | C | D. | D |
3.下列有关物质用途的说法错误的是( )
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 工业上用石灰对煤燃烧后形成的烟气进行脱硫,并能回收到石膏 | |
| C. | 单质硅可用于制半导体、光导纤维等 | |
| D. | 氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 |
4.分子式为C6H12O2的酯共有(不考虑立体异构)( )
| A. | 18种 | B. | 19种 | C. | 20种 | D. | 21种 |
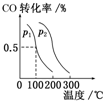 联合国气候变化大会于2009年12月7~18日在哥本哈根召开.中国政府承诺到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.
联合国气候变化大会于2009年12月7~18日在哥本哈根召开.中国政府承诺到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.