题目内容
5.新华网北京12月17日电 公安部17日公布了新修改的《机动车驾驶证申领和使用规定》,2010年4月1日起施行.其中,饮酒后驾驶机动车,由一次记6分调整为记12分.酒后驾车是引发交通事故的重要原因,交警对驾驶员进行呼气酒精(乙醇)检测的原理是:橙色的K2Cr2O7酸性溶液与乙醇反应生成蓝绿色Cr3+.下列有关叙述正确的是( )①K2Cr2O7是氧化剂 ②乙醇表现氧化性和还原性
③Cr3+是还原产物 ④闻气味能判断是否酒后驾车.
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ②④ |
分析 橙色的K2Cr2O7酸性溶液与乙醇反应生成蓝绿色Cr3+.可知,Cr元素的化合价降低,乙醇中C元素的化合价升高,以此来解答.
解答 解:①由信息可知,Cr元素的化合价降低,则K2Cr2O7是氧化剂,故正确;
②乙醇在反应中失去电子,只体现还原性,故错误;
③Cr得到电子被还原,则Cr3+是还原产物,故正确;
④该原理说明不能利用闻气味能判断是否酒后驾车,故错误;
故选A.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及应用能力的考查,题目难度不大.

练习册系列答案
相关题目
15.下列反应的离子方程式,正确的是( )
| A. | 用小苏打治疗胃酸过多:CO${\;}_{3}^{2-}$+2H+═CO2↑+H2O | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 用FeCl3溶液腐蚀印刷电路板上铜箔:Fe3++Cu═Fe2++Cu2+ | |
| D. | 钠与氢氧化钠溶液反应:2Na+2H2O═2Na++2OH-+H2↑ |
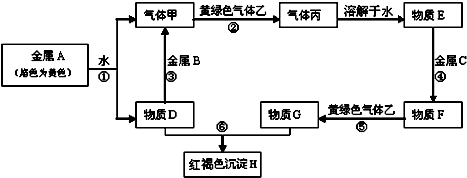
13.以苯、硫酸、氢氧化钠、亚硫酸钠为原料,经典的合成苯酚的方法可简单表示为:

有关说法错误的是( )

有关说法错误的是( )
| A. | 第②步反应的化学方程式为: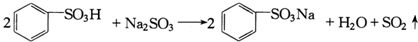 | |
| B. | 第③步反应中除了苯酚钠还会生成Na2SO4 | |
| C. | 第④步反应可表示为: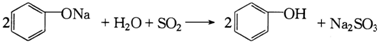 | |
| D. | 根据上述反应判断酸性强弱为: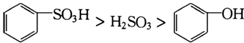 |
20.下列离子方程式正确的是( )
| A. | 铁跟FeCl3溶液反应:Fe+Fe3+═2Fe2+ | |
| B. | 金属铝溶于氢氧化钠溶液:Al+2OH-═AlO2-+H2↑ | |
| C. | FeCl2溶液跟Cl2反应:Fe2++Cl2═Fe3++2Cl- | |
| D. | Fe(OH)3跟盐酸反应:Fe(OH)3+3H+═Fe3++3H2O |
10.下列化合物与其性质或用途相符的是( )
| A. | 漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 | |
| B. | Na2SiO3是不溶于水的盐,可作硅胶 | |
| C. | 二氧化硅是制造光导纤维的材料 | |
| D. | 实验室用带玻璃塞的试剂瓶保存氢氧化钠溶液 |
14.下列物质中,不能用玻璃瓶来盛装的是( )
| A. | 烧碱溶液 | B. | 浓硫酸 | C. | 氢氟酸 | D. | 碳酸钠溶液 |
15.利用图示装置进行有关实验,其中能达到实验目的或得出正确结论的是( )
| 选项 | 3 | ② | ③ | ④ | 实验目的或结论 | 装置 |
| A | 浓盐酸 | MnO2 | 干燥红色布条 | NaOH溶液 | 干燥布条不褪色 |  |
| B | 浓硫酸 | NaCl粉末 | 空气 | NaOH溶液 | 制备收集HCl | |
| C | 浓硝酸 | 木炭 | 空气 | NaOH溶液 | 浓硝酸具有氧化性 | |
| D | 浓氨水 | NaOH固体 | 空气 | 水 | 制备收集氨气 |
| A. | A | B. | B | C. | C | D. | D |