题目内容
11. SO2的催化氧化是工业制取硫酸的关键步骤之一,该反应的化学方程式为:2SO2+O2$?_{△}^{催化剂}$2SO3.请回答下列问题:
SO2的催化氧化是工业制取硫酸的关键步骤之一,该反应的化学方程式为:2SO2+O2$?_{△}^{催化剂}$2SO3.请回答下列问题:(1)已知1mol SO2(g)生成1mol SO3(g)的能量变化如下图所示(E1、E2均为正值)
①图中A、C分别表示1mol SO2和0.5mol氧气的能量、1mol SO3能量.
②2SO2(g)+O2(g)?2SO3(g)△H=-2(E2-E1)kJ/mol(用含“E1”、“E2”的代数式表示).
③已知:在一定条件下,64g SO2气体氧化为SO3气体时放出99kJ的热量,请写出SO2氧化为SO3的热化学方程式2SO2(g)+O2(g)=2SO3(g)△H=-198KJ•mol-1 .
(2)判断该反应在恒温、恒容时达到平衡状态的标志是BC(填字母).
A.SO2和SO3浓度相等 B.SO2百分含量保持不变
C.容器中气体的压强不变 D.SO3的生成速率与SO2的消耗速率相等
(3)当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的是A(填字母).
A.向装置中再充入O2 B.向装置中再充入SO2
C.改变反应的催化剂 D.升高温度
(4)将0.060mol SO2(g)和0.040mol O2(g)放入容积为1L的密闭容器中,在一定条件下达到平衡,测得c(SO3)=0.040mol/L.计算该条件下反应的平衡常数K和SO2的转化率(不必写出计算过程).
①平衡常数K=200(mol?L-1)-1.
②平衡时,SO2的转化率 α(SO2)=66.7%.
分析 (1)①A表示反应物总能量,C表示生成物总能量;
②反应物总能量高于生成物总能量,为放热反应,由图可知1mol二氧化硫放出能量为E2-E1,2SO2(g)+O2(g)?2SO3(g)的反应热表示2mol二氧化硫放出的能量;
③2mol二氧化硫氧化为三氧化硫方程式的热量为99kJ×$\frac{2mol×64g/mol}{64g}$=198kJ,注明物质的聚集状态与反应热书写热化学方程式;
(2)可逆反应到达平衡时,同种物质的正逆速率相等,各组分的浓度、含量保持不变,由此衍生的其它一些量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不再变化说明到达平衡;
(3)提高SO2平衡转化率,改变条件应使平衡正向移动,但不能只增大二氧化硫的浓度;
(4)将0.060mol SO2(g)和0.040mol O2(g)放入容积为1L的密闭容器中,在一定条件下达到平衡,测得c(SO3)=0.040mol/L,则:
2SO2(g)+O2(g)?2SO3(g)
起始浓度(mol/L):0.06 0.04 0
变化浓度(mol/L):0.04 0.02 0.04
平衡浓度(mol/L):0.02 0.02 0.04
①代入K=$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{3})×c({O}_{2})}$计算平衡常数;
②转化率=$\frac{浓度变化量}{起始浓度}$×100%.
解答 解:(1)①A表示1mol SO2和0.5mol氧气的能量,C表示生成物总能量;
故答案为:1mol SO2和0.5mol氧气的能量;1mol SO3能量;
②反应物总能量高于生成物总能量,为放热反应,由图可知1mol二氧化硫放出能量为E2-E1,故反应2SO2(g)+O2(g)?2SO3(g)的△H=-2(E2-E1)kJ/mol,
故答案为:-2(E2-E1)kJ/mol;
③2mol二氧化硫氧化为三氧化硫方程式的热量为99kJ×$\frac{2mol×64g/mol}{64g}$=198kJ,热化学方程式为:2SO2(g)+O2(g)=2SO3(g)△H=-198KJ•mol-1 ,
故答案为:2SO2(g)+O2(g)=2SO3(g)△H=-198KJ•mol-1 ;
(2)A.平衡时SO2和SO3浓度关系与二氧化硫转化率有关,不一定相等,故A错误;
B.SO2百分含量保持不变,说明到达平衡,故B正确;
C.随反应进行,混合气体总物质的量进行,恒温恒容下容器内压强减小,当容器中气体的压强不变,说明到达平衡,故C正确;
D.SO3的生成速率与SO2的消耗速率均表示正反应速率,反应始终相等,不能说明到达平衡,SO3的生成速率与SO2的生成速率相等,说明到达平衡,故D错误,
故选:BC;
(3)A.向装置中再充入O2,氧气浓度增大,平衡正向移动,SO2平衡转化率增大,故A正确;
B.向装置中再充入SO2,SO2平衡转化率减小,故B错误;
C.改变反应的催化剂,不影响平衡移动,SO2平衡转化率不变,故C错误;
D.正反应为放热反应,升高温度,平衡逆向移动,SO2平衡转化率减小,故D错误,
故选:A;
(4)将0.060mol SO2(g)和0.040mol O2(g)放入容积为1L的密闭容器中,在一定条件下达到平衡,测得c(SO3)=0.040mol/L,则:
2SO2(g)+O2(g)?2SO3(g)
起始浓度(mol/L):0.06 0.04 0
变化浓度(mol/L):0.04 0.02 0.04
平衡浓度(mol/L):0.02 0.02 0.04
①则平衡醋酸是K=$\frac{{c}^{2}(S{O}_{3})}{{c}^{2}(S{O}_{3})×c({O}_{2})}$=$\frac{0.0{4}^{2}}{0.0{2}^{2}×0.02}$(mol?L-1)-1=200(mol?L-1)-1,故答案为:200(mol?L-1)-1;
②平衡时,SO2的转化率 α(SO2)=$\frac{0.04mol/L}{0.06mol/L}$×100%=66.7%,故答案为:66.7%.
点评 本题考查化学平衡计算与影响因素、平衡状态判断、化学反应中能量变化、热化学方程式书写等,需要学生熟练掌握基础知识并能灵活应用.

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案| A. | 1904年,道尔顿提出了一个被称为“葡萄干面包式”的原子结构模型 | |
| B. | 在化学反应过程中,原子最外层电子数不发生变化,但原子核可能会发生变化 | |
| C. | 在活泼金属与活泼非金属的反应中,金属元素的原子得到电子,表现为负化合价 | |
| D. | 原子不带电,原子的质量主要集中在原子核上 |
| 阳离子 | K+ Cu2+ Fe3+ Al3+ Fe2+ |
| 阴离子 | Cl- CO${\;}_{3}^{2-}$ NO${\;}_{3}^{-}$ SO${\;}_{4}^{2-}$ SiO${\;}_{3}^{2-}$ |
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
Ⅱ.取少量溶液于试管中,加入KSCN溶液后无明显变化.
Ⅲ.另取少量溶液于试管中,加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+(写离子符号).
(2)甲同学最终确定原溶液中所含阴离子是Cl-、NO3-、SO42-(写离子符号).
(3)Ⅲ中加入少量盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+═3Fe3++NO+2H2O.
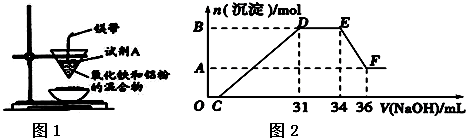
(4)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为1.6g.
(5)工业废水中常含有不同类型的污染物,可采用不同的方法处理.以下是乙同学针对含不同污染物的废水提出的处理措施和方法,其中正确的是D.
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 废酸 | 加生石灰中和 | 物理法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含复杂有机物的废水 | 通过微生物代谢 | 物理法 |
| D | 碱性的废水 | 用CO2中和 | 化学法 |
 在某一容积为5L的密闭容器内,加入0.2mol的CO和0.2mol的H2O,在催化剂存在的条件下高温加热,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g).反应中CO2的浓度随时间变化情况如图:
在某一容积为5L的密闭容器内,加入0.2mol的CO和0.2mol的H2O,在催化剂存在的条件下高温加热,发生如下反应:CO(g)+H2O(g)?CO2(g)+H2(g).反应中CO2的浓度随时间变化情况如图: