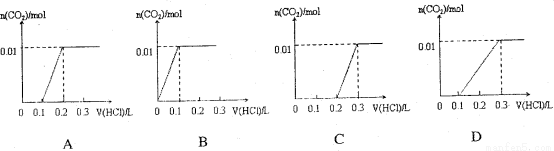
题目内容
下列有关NH4Fe(SO4)2水溶液的叙述正确的是
A.该溶液中Mg2+、H+、NO3-、Cl-可以大量共存
B.该溶液能使碘化钾试纸变蓝,反应的离子方程式为:Fe3++2I-=Fe2++I2
C.该溶液和足量的Ba(OH)2溶液反应的离子方程式为: Fe3++SO42-+Ba2++3OH-=BaSO4↓+Fe(OH)3↓
D. 该溶液与足量铜粉 反应的离子方程式为:2Fe3++3Cu=2Fe+3Cu2+
练习册系列答案
相关题目
4.下列关于铁制品腐蚀或保护措施的说法中不正确的有( )
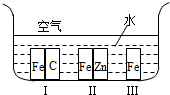

| A. | 在如图所示环境中,铁被腐蚀速率:Ⅰ>Ⅲ>Ⅱ | |
| B. | 军事演习期间给坦克的履带上刷上油漆以防止生锈 | |
| C. | 在海轮的外壳上常焊有锌块,且定期更新 | |
| D. | 将不锈钢制成刀具和餐具,有的刀具还进行烤蓝处理 |
下列有关实验操作、现象和解释或结论都正确的是
选项 | 实验操作 | 现象 | 解释或结论 |
A | 过量的Fe粉中加入稀硝酸,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀硝酸将Fe氧化为Fe3+ |
B | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
C | 铝箔插入稀硝酸中 | 无现象 | 铝箔表面被HNO3氧化,形成致密的氧化膜 |
D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |




 3Mg+Al2O3
3Mg+Al2O3