题目内容
某铜矿主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以此铜矿石为原料制备CuSO4·5H2O及CaCO3,部分步骤如下:
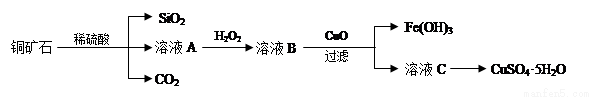
请回答下列问题:
(1)溶液A除含有Cu2+外,还可能含有的金属离子有________(填离子符号);验证所含离子所用的试剂是在__________。
(2)可用生成的CO2制取优质碳酸钙。制备时,先向氯化钙溶液中通入氨气,再通入CO2。
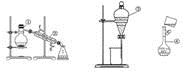
①实验室通常采用加热氯化铵和氢氧化钙混合物的方法制取氨气。某学习小组选取下图所给部分装置制取并收集纯净的氨气。

如果按气流方向连接各仪器接口,你认为正确的顺序为
a→_________、_________→_________、_________→i。
其中与i相连漏斗的作用是______________。
②为探究氨气和氯气的反应
a. 装置A、B,B装置内的药品依次是____________、____________。
b.装置C可用于探究氯气与氨气(已知氯气和氨气可发生反应:3Cl2+2NH3=N2+6HCl)的反应。实验打开开关1、3,关闭2,先向烧瓶中通入____________,然后关闭1、3,打开2,向烧瓶中缓缓通入一定量的另一种气体。实验一段时间后向烧瓶内出现浓厚的白烟并在容器内壁凝结。

(3)测定铜矿石中Cu2(OH)2CO3质量百分含量的方法是:
a.将1.25g铜矿石制取的CuSO4·5H2O于锥形瓶中,加入适量水完全溶解;
b.向溶液中加入100mL0.25mol/L的氢氧化钠溶液使Cu2+完全沉淀;
c.过滤;
d.滤液中的氢氧化钠溶液用0.5mol/L盐酸滴定至终点,耗用10mL盐酸。则铜矿石中Cu2(OH)2CO3质量分数为_____________。
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目


 (写结构简式)
(写结构简式)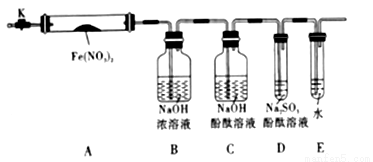
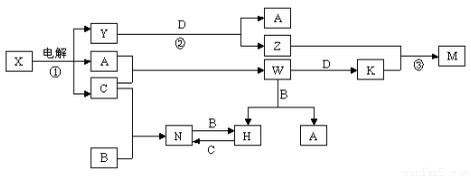
 、B、C、D是单质,其余是化合物。其中B、D是常见金属。又知A在C中点燃有苍白色火焰,M既可溶于盐酸又可溶于NaOH溶液。请回答下列问题:
、B、C、D是单质,其余是化合物。其中B、D是常见金属。又知A在C中点燃有苍白色火焰,M既可溶于盐酸又可溶于NaOH溶液。请回答下列问题: 。
。 3)写出下列反应的离子方程式:
3)写出下列反应的离子方程式: