题目内容
7.下列关于金属钠的叙述正确的是( )| A. | 金属钠可以保存在煤油或酒精中,防止在空气中变质 | |
| B. | 钠是强氧化剂 | |
| C. | 钠与熔融的四氣化钛反应可制取钛 | |
| D. | 实验时用剩的钠块不应放回原试剂瓶 |
分析 A.钠和酒精反应生成氢气;
B.金属只能失电子做还原剂;
C.钠的还原性强,钠能与熔融状态下的四氯化钛反应制取金属钛;
D.实验时用剩的钠块应该放回原瓶.
解答 解:A.钠较活泼,易和水、氧气反应而变质,煤油和钠不反应且密度小于钠,所以煤油可以保存钠;钠和乙醇反应生成乙醇钠和氢气,所以不能用乙醇保存钠,故A错误;
B.钠反应中失电子做还原剂,故B错误;
C.钠的还原性强,可用钠和熔融状态下的四氯化钛反应制取金属钛,故C正确;
D.钠是活泼金属易和空气中氧气、水蒸气等发反应,不能随意乱丢弃,实验时用剩的钠块应该放回原瓶,故D错误.
故选C.
点评 本题涉及金属钠的保存以及性质等知识,注意知识的归纳和整理是关键,题目难度不大.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
8.下列有关物质用途的描述不正确的是( )
| A. | 氧化铁可制作防锈油漆 | |
| B. | 碳酸氢钠可制作焙制糕点的发酵粉 | |
| C. | 氯气不能用来合成药物,因为它有毒 | |
| D. | NO能促进血管扩张,防止血管栓塞 |
9.用向上排空气法在烧瓶中收集氯化氢气体,一段时间后烧瓶中气体的相对分子质量是34.6,现将烧瓶置于水中,最后进入烧瓶的溶液的体积约占烧瓶体积的( )
| A. | 0 | B. | $\frac{1}{4}$ | C. | $\frac{1}{2}$ | D. | $\frac{3}{4}$ |
15.将9.6gCu投入到一定浓度的HNO3溶液中,恰好完全反应,产生NO2 和NO的混合气体共5.6L(标况下).则原溶液中HNO3 的物质的量为( )
| A. | 0.18mol | B. | 0.25mol | C. | 0.36mol | D. | 0.55mol |
2.把7.2g铁粉投入40ml某浓度的硝酸中,充分反应后剩余固体1.6g,产生NO2和NO的混合气体0.08mol.若不考虑N2O4的存在,则该硝酸的物质的量浓度为( )
| A. | 3.5mol•L-1 | B. | 7.0mol•L-1 | C. | 4.5mol•L-1 | D. | 9.0mol•L-1 |
12.下列溶液中的Cl-浓度与150mL1mol•L-1MgCl2溶液中的Cl-浓度相等的是( )
| A. | 150mL1mol•L-1NaCl溶液 | B. | 100mL2mol•L-1KCl溶液 | ||
| C. | 75mL0.5mol•L-1CaCl2溶液 | D. | 75mL1mol•L-1AlCl3溶液 |
19.下列粒子的核外电子排布正确的是( )
| A. | Na  | B. | K  | C. | Xe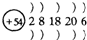 | D. | Cl- |
16.下列说法正确的是( )
| A. | 明矾可用作净水剂 | B. | 在铝热反应中氧化铝是氧化剂 | ||
| C. | 氢氧化铝能溶于氨水 | D. | 氧化铝与水反应可制得氢氧化铝 |
17.已知铋(Bi)元素的化合价可表现为+3或+5价.锗酸铋(简称BGO)是我国研制成功的一种性能优良的闪烁晶体材料,其中的锗(Ge)元素为+4价.BGO可看成由锗和铋两种元素的氧化物所形成的复杂化合物,已知在BGO中两种氧化物所含氧的质量相同,则BGO的化学式可能是( )
| A. | Bi3Ge3O15 | B. | Bi3Ge3O12 | C. | Bi4Ge3O16 | D. | Bi4Ge3O12 |