题目内容
下表为元素周期表前四周期的一部分,下列叙述正确的是( )


| A、Y单质在空气中燃烧生成YO3 |
| B、Z元素的最高价氧化物的水化物酸性最强 |
| C、X的氢化物为H2X |
| D、Y、Z和W的阴离子半径依次增大 |
考点:原子结构与元素的性质,原子结构与元素周期律的关系
专题:
分析:由短周期元素在周期表中位置,可知X为N元素、Y为S元素、Z为Cl、W为Br、R为Ar,D中离子半径比较规律:电子层结构相同、核电荷数越大离子半径越小,电子层越多离子半径越大,结合元素化合物性质解答.
解答:
解:由短周期元素在周期表中位置,可知X为N元素、Y为S元素、Z为Cl、W为Br、R为Ar.
A.硫单质在空气中燃烧生成SO2,故A错误;
B.Z元素的最高价氧化物的水化物为高氯酸,其酸性最强,故B正确;
C.X的氢化物为NH3,故C错误;
D.电子层结构相同、核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径Br->S2->Cl-,故D错误,
故选B.
A.硫单质在空气中燃烧生成SO2,故A错误;
B.Z元素的最高价氧化物的水化物为高氯酸,其酸性最强,故B正确;
C.X的氢化物为NH3,故C错误;
D.电子层结构相同、核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径Br->S2->Cl-,故D错误,
故选B.
点评:本题考查元素周期表、元素周期律等,比较基础,注意理解掌握微粒半径比较,有利于对基础知识的巩固.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
化学在工农业生产和日常生活中有着重要的应用.下列叙述正确的是( )
| A、雾霾天气对人的健康造成危害,“雾”和“霾”的分散质微粒相同 |
| B、“辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料 |
| C、浸泡过高锰酸钾溶液的硅土可用于鲜花和水果的保鲜 |
| D、“84”消毒液和洁厕灵可以混合使用,以达到更好的去污效果 |
化学与能源开发、环境保护、生产生活等密切相关.下列叙述错误的是( )
| A、光催化水制氢比电解水制氢更节能环保 |
| B、用聚乙烯塑料代替聚乳酸塑料可减少白色污染 |
| C、开发利用可再生能源,可减少化石燃料的使用 |
| D、改进汽车尾气净化技术,可减少大气污染物的排放 |
 高铁酸盐在能源环保领域有广泛用途.用镍(Ni),铁做电极电解浓氢氧化钠溶液制备Na2FeO4的装置如图,说法合理的是( )
高铁酸盐在能源环保领域有广泛用途.用镍(Ni),铁做电极电解浓氢氧化钠溶液制备Na2FeO4的装置如图,说法合理的是( )| A、镍是阳极,电极反应4OH--4e-=2H2O+O2↑ |
| B、电解时电流方向:负极→镍电极→溶液→铁电极→正极 |
| C、若隔膜是阴离子交换膜,则OH-自右向左移动 |
| D、电解时阳极区pH降低,阴极区pH升高,撤去隔膜后与原溶液比较pH降低(假设电解前后体积变化忽略不计) |
 国庆期间对大量鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,说法正确的是( )
国庆期间对大量鲜花施用了S-诱抗素制剂,以保证鲜花盛开.S-诱抗素的分子结构如图,说法正确的是( )| A、分子式C15H21O4 |
| B、既能发生加聚反应,又能发生缩聚反应 |
| C、分子中有两个手性碳原子 |
| D、既能使氯化铁溶液发生显色反应,又能使酸性高锰酸钾溶液褪色 |
在25℃时,下列溶液的pH或微粒的物质的量浓度关系正确的是( )
| A、将0.2mol/L的某一元酸HA溶液和0.1mol/L NaOH溶液等体积混合后溶液pH大于7,则充分反应后的混合液:2c(OH-)=2c(H+)+c(HA)-c(A-) |
| B、某溶液中存在的离子有S2-、HS-、OH-、Na+、H+,则离子浓度的大小关系一定是:c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+) |
| C、将pH=4的醋酸溶液与pH=10的KOH溶液等体积混合,则充分反应后的混合液:c(CH3COO-)>c(H+)>c(K+)>c(OH-) |
| D、某物质的溶液中由水电离出c(H+)=1×10-amol/L,若a>7时,则该溶液的pH一定为14-a |
下列说法或表述中正确的是( )
A、烷烃 的系统命名为2-甲基-2-乙基丙烷 的系统命名为2-甲基-2-乙基丙烷 |
| B、由石油分馏可以获得石蜡,由石蜡裂化可获得乙烯 |
C、如图所示的有机物分子式为C14H12O2,能发生银镜反应 |
| D、在碱性条件下,CH3CO18OC2H5的水解产物是CH3COOH和C2H518OH |
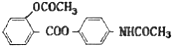 ,其合成途径如下:
,其合成途径如下: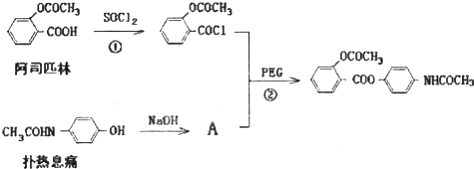 完成下列填空:
完成下列填空: