题目内容
4.下列反应中通入的气体只做氧化剂的是( )| A. | SO2通入H2S溶液中 | B. | Cl2通入NaOH溶液 | ||
| C. | SO2通入KOH溶液中 | D. | H2S通入溴水中 |
分析 通入的气体只做氧化剂,则气体中某元素的化合价降低,以此来解答.
解答 解:A.反应生成S和水,二氧化硫中S元素的化合价降低,作氧化剂,故A选;
B.反应生成氯化钠、次氯酸钠,Cl元素的化合价升高也降低,则氯气为氧化剂也为还原剂,故B不选;
C.反应生成亚硫酸钾和水,或生成亚硫酸氢甲,无元素的化合价变化,故C不选;
D.反应生成S和HBr,S元素的化合价升高,则气体作还原剂,故D不选;
故选A.
点评 本题考查氧化还原反应,为高频考点,把握发生的反应及元素的化合价变化为解答的关键,侧重分析与应用能力考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列反应的离子方程式正确的是( )
| A. | 大理石与盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 在氯化铝溶液中滴加过量的氨水:Al3++4 OH-═[Al (OH)4]- | |
| C. | 在氢氧化钠溶液中通入过量的CO2:2OH-+CO2═CO32-+H2O | |
| D. | 二氧化硅与苛性钠溶液反应:SiO2+2OH-═SiO32-+H2O |
19.下列各物质中酸性最弱的是( )
| A. | H2SiO3 | B. | HClO4 | C. | H2SO4 | D. | H2CO3 |
9.下列关于甲烷与Cl2的取代反应所得产物的说法正确的是( )
| A. | 都是有机物 | B. | 都不溶于水 | ||
| C. | 有一种气态物质,其余均是液体 | D. | 除一种外均是四面体结构 |
16.下列物质中,属于共价化合物的是( )
| A. | MgCl2 | B. | HCl | C. | NH4Cl | D. | Na2O2 |
 .
.
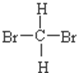 和
和
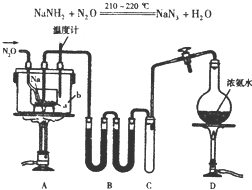 NaN3(叠氮化钠)是一种易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,常用作汽车安全气囊中的药剂.实验室制取叠氮化钠的原理、实验装置及步骤如下:
NaN3(叠氮化钠)是一种易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,常用作汽车安全气囊中的药剂.实验室制取叠氮化钠的原理、实验装置及步骤如下: