题目内容
下列实验中操作、现象、结论对应关系正确的一组是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 在蔗糖中加入几滴水搅拌均匀,再加入浓硫酸,迅速搅拌 | 蔗糖逐渐变黑,体积膨胀,形成疏松多孔的物质 | 只体现了浓硫酸的脱水性 |
| B | 淀粉和稀硫酸混合共热后,再加少量新制氢氧化铜悬浊液 | 产生红色沉淀 | 淀粉水解可生成葡萄糖 |
| C | 溴乙烷和氢氧化钠溶液充分反应后,用足量稀硝酸酸化,再加入硝酸银溶液 | 生成淡黄色沉淀 | 溴乙烷中含有溴元素 |
| D | 将溴水加入苯中并充分振荡 | 溴水褪色 | 苯与溴发生了取代反应 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.蔗糖逐渐变黑,体积膨胀,形成疏松多孔的物质,生成碳、二氧化硫、二氧化碳等,以此判断;
B.与氢氧化铜的反应应在碱性条件下进行;
C.溴乙烷和氢氧化钠溶液中水解,检验溴离子应在酸性条件下;
D.苯和溴水不反应.
B.与氢氧化铜的反应应在碱性条件下进行;
C.溴乙烷和氢氧化钠溶液中水解,检验溴离子应在酸性条件下;
D.苯和溴水不反应.
解答:
解:A.蔗糖逐渐变黑,体积膨胀,形成疏松多孔的物质,生成碳、二氧化硫、二氧化碳等,反应中浓硫酸起到脱水性和强氧化性的作用,故A错误;
B.淀粉在酸性条件下水解生成葡萄糖,葡萄糖与氢氧化铜的反应应在碱性条件下进行,反应后用加入碱条件溶液呈碱性,否则不能生成砖红色沉淀,故B错误;
C.溴乙烷和氢氧化钠溶液中水解,检验溴离子应在酸性条件下,故C正确;
D.苯和溴水不反应,应和液溴在溴化铁催化作用下反应,故D错误.
故选C.
B.淀粉在酸性条件下水解生成葡萄糖,葡萄糖与氢氧化铜的反应应在碱性条件下进行,反应后用加入碱条件溶液呈碱性,否则不能生成砖红色沉淀,故B错误;
C.溴乙烷和氢氧化钠溶液中水解,检验溴离子应在酸性条件下,故C正确;
D.苯和溴水不反应,应和液溴在溴化铁催化作用下反应,故D错误.
故选C.
点评:本题考查较为综合,涉及浓硫酸的性质、淀粉的水解、溴乙烷的水解以及苯的性质,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质以及实验的严密性的评价,难度中等.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
在恒温下,密闭容器中的可逆反应:2SO3(气)?2SO2(气)+O2(气)可用来确定该反应已经达到平衡状态的是( )
| A、反应容器内,压强不随时间改变 |
| B、单位时间消耗1molSO3同时生成1molSO2 |
| C、单位时间消耗1molSO3同时消耗1molSO2 |
| D、容器内混合气体的总质量不发生变化 |
类比推断是学习化学的一种重要方法.下列推断正确的是( )
| A、NO和NO2的密度都比空气大,都可以用向上排空气法收集 |
| B、丙烷和乙醇的分子量相近,二者沸点也相近 |
| C、SO2和CO2都是酸性氧化物,都能与KOH溶液反应 |
| D、Na2O和Na2O2所含元素相同,故与CO2反应产物也相同 |
贮满干燥的种气体的试管倒置于水中,轻轻振荡,水可以充满试管的三分之二.该气体是( )
| A、N2 |
| B、NO2 |
| C、O2 |
| D、H2 |
在给定条件的水溶液中一定能大量共存的离子组是( )
| A、含有SO42-的溶液:Ca2+、NH4+、HCO3-、Cl- |
| B、c(Fe2+)=0.5 mol/L的溶液:H+、Na+、Cl-、SO42- |
| C、pH=1的溶液:Na+、K+、Cl-、CO32- |
| D、酸性无色透明溶液中:Fe2+、Na+、NO3-、CO32- |
下列说法正确的是( )
A、按系统命名法,化合物 的名称为2,4-二乙基-6-丙基辛烷 的名称为2,4-二乙基-6-丙基辛烷 |
B、DDT的结构简式为 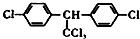 ,分子中最多有14个碳原子共平面 ,分子中最多有14个碳原子共平面 |
| C、醋酸和硬脂酸互为同系物,C2H6和C9H20也一定互为同系物 |
D、结构片段为 的高聚物,是其单体通过缩聚反应生成 的高聚物,是其单体通过缩聚反应生成 |
以NA表示阿伏加德罗常数,下列说法中正确的是( )
| A、1.8g NH4+离子中含有的电子数为NA |
| B、常温常压下,1mol甲基(-CH3)所含电子数为10NA |
| C、25℃,1.01×105 Pa下,使V L氯化氢气体溶于水得V L水溶液,所得溶液的物质的量浓度为1/22.4 mol?L-1 |
| D、标准状况下,22.4 L Cl2和HCl的混合气体中含分子总数为2NA |
若一氧化碳和二氧化碳的混合气体的密度与同温同压下氧气的密度相同,混合气体中一氧化碳和二氧化碳的物质的量之比是( )
| A、1:3 | B、3:1 |
| C、2:1 | D、1:2 |
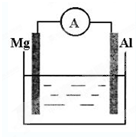 如图所示,组成一个原电池.
如图所示,组成一个原电池.