题目内容
在给定条件的水溶液中一定能大量共存的离子组是( )
| A、含有SO42-的溶液:Ca2+、NH4+、HCO3-、Cl- |
| B、c(Fe2+)=0.5 mol/L的溶液:H+、Na+、Cl-、SO42- |
| C、pH=1的溶液:Na+、K+、Cl-、CO32- |
| D、酸性无色透明溶液中:Fe2+、Na+、NO3-、CO32- |
考点:离子共存问题
专题:离子反应专题
分析:A.钙离子与硫酸根离子反应生成硫酸钙沉淀;
B.H+、Na+、Cl-、SO42-离子之间不满足离子反应发生条件,都不与亚铁离子反应;
C.pH=1的溶液为酸性溶液,碳酸根离子能够与氢离子反应;
D.亚铁离子为有色离子,亚铁离子与碳酸根离子反应、酸性条件下硝酸根离子能够氧化亚铁离子.
B.H+、Na+、Cl-、SO42-离子之间不满足离子反应发生条件,都不与亚铁离子反应;
C.pH=1的溶液为酸性溶液,碳酸根离子能够与氢离子反应;
D.亚铁离子为有色离子,亚铁离子与碳酸根离子反应、酸性条件下硝酸根离子能够氧化亚铁离子.
解答:
解:A.SO42-、Ca2+离子之间反应生成沉淀硫酸钙,在溶液中不能大量共存,故A错误;
B.H+、Na+、Cl-、SO42-之间不反应,且都不与Fe2+反应,在溶液中能够大量共存,故B正确;
C.该溶液为酸性溶液中,溶液中存在大量氢离子,CO32-与氢离子反应,在溶液中不能大量共存,故C错误;
D.Fe2+为有色离子,Fe2+与酸性条件下的NO3-发生氧化还原反应,CO32-与Fe2+、H+反应,在溶液中不能大量共存,故D错误;
故选B.
B.H+、Na+、Cl-、SO42-之间不反应,且都不与Fe2+反应,在溶液中能够大量共存,故B正确;
C.该溶液为酸性溶液中,溶液中存在大量氢离子,CO32-与氢离子反应,在溶液中不能大量共存,故C错误;
D.Fe2+为有色离子,Fe2+与酸性条件下的NO3-发生氧化还原反应,CO32-与Fe2+、H+反应,在溶液中不能大量共存,故D错误;
故选B.
点评:本题考查离子共存的正误判断,为中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
将盛满NO2和O2混合气体的试管倒立于水中,经过足够长的时间后,试管内气体体积缩小为原体积的一半,则剩余气体的成分是( )
| A、NO或O2 |
| B、NO |
| C、O2 |
| D、NO2 |
阿司匹林是一种常见药物,它的相对分子质量为180,含碳、氢、氧三种元素,其中碳、氢的质量数分别是60%、4.4%,则阿司匹林的分子式是( )
| A、C10H9O4 |
| B、C 10H22O3 |
| C、C9H10O4 |
| D、C9H8O4 |
常温下,下列不能共存的分子组( )
| A、N2、O2、CO2、H2 |
| B、N2、H2、H2O(g)、CO |
| C、NH3、Cl2、HCl、H2 |
| D、CO、CO2、O2、HCl |
取含有 0.02mol 的硫酸溶液,先投入 0.24g 镁粉,再滴入NaOH 溶液,当使溶液中的镁离子全部转化为沉淀时,需要NaOH的物质的量为( )
| A、0.02mol |
| B、0.03mol |
| C、0.04mol |
| D、0.01mol |
下列实验装置或操作正确的是( )
A、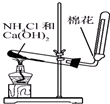 制取氨气 |
B、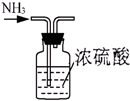 干燥氨气 |
C、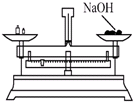 称量NaOH固体 |
D、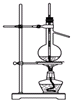 石油的分馏 |
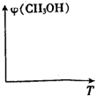 工业上在合成塔中采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H=QkJ/mol
工业上在合成塔中采用下列反应合成甲醇:CO(g)+2H2(g)?CH3OH(g)△H=QkJ/mol