题目内容
19.下列物质溶于水后,抑制了水的电离的是( )| A. | Na2CO3 | B. | NH4Cl | C. | CH3COONa | D. | H2SO4 |
分析 酸或碱抑制水电离,含有弱离子的盐促进水电离,物质溶于水后能使水的电离程度增大,以此解答该题.
解答 解:A.Na2CO为强碱弱酸盐,水解呈碱性,促进水的电离,故A不选;
B.NH4Cl为强酸弱碱盐,水解呈酸性,促进水的电离,故B不选;
C.CH3COONa为强碱弱酸盐,水解呈碱性,促进水的电离,故C不选;
D.硫酸电离出氢离子,溶液中氢离子浓度增大,抑制水的电离,故D选.
故选D.
点评 本题以电解质的电离、盐类的水解为载体考查水的电离,为高频考点,明确溶液中溶质及其性质是解本题关键,题目难度不大.

练习册系列答案
相关题目
15. 合成氨工业对国民经济和社会发展具有重要的意义.对于一定体积密闭容器中的反应:N2(g)+3H2(g)?NH3(g)(正反应为放热反应),673K、30MP下,n (NH3)和n (H2)随时间t变化的关系如图所示.下列叙述中,不正确的是( )
合成氨工业对国民经济和社会发展具有重要的意义.对于一定体积密闭容器中的反应:N2(g)+3H2(g)?NH3(g)(正反应为放热反应),673K、30MP下,n (NH3)和n (H2)随时间t变化的关系如图所示.下列叙述中,不正确的是( )
 合成氨工业对国民经济和社会发展具有重要的意义.对于一定体积密闭容器中的反应:N2(g)+3H2(g)?NH3(g)(正反应为放热反应),673K、30MP下,n (NH3)和n (H2)随时间t变化的关系如图所示.下列叙述中,不正确的是( )
合成氨工业对国民经济和社会发展具有重要的意义.对于一定体积密闭容器中的反应:N2(g)+3H2(g)?NH3(g)(正反应为放热反应),673K、30MP下,n (NH3)和n (H2)随时间t变化的关系如图所示.下列叙述中,不正确的是( )| A. | 点c处正反应速率比逆反应速率大 | |
| B. | 点a的正反应速率比点b的正反应速率大 | |
| C. | 气体的平均摩尔质量:点b大于点a | |
| D. | 混合气体的密度:点b大于点a |
10. 某化学兴趣设计实验制取乙酸乙酯.现用右图装置进行实验,在圆底烧瓶内加入碎瓷片,再加入由2ml 98%的浓H2SO4和3mL乙醇组成的混合液,通过分液漏斗向烧瓶内加入2mL醋酸,烧杯中加入饱和Na2CO3溶液.请回答下列问题:
某化学兴趣设计实验制取乙酸乙酯.现用右图装置进行实验,在圆底烧瓶内加入碎瓷片,再加入由2ml 98%的浓H2SO4和3mL乙醇组成的混合液,通过分液漏斗向烧瓶内加入2mL醋酸,烧杯中加入饱和Na2CO3溶液.请回答下列问题:
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH.
②有关有机物的沸点:
(1)该实验有机反应物中含有的官能团有羟基、羧基(填写名称)若用同位素18O示踪法确定反应产物水分子中氧原子的提供者(设18O在CH3CH2OH中),写出能表示18O位置的化学方程式CH3COOH+CH3CH218OH $?_{△}^{浓硫酸}$CH3CO18OC2H5+H2O,反应类型是酯化反应(取代反应).
(2)与书中采用的实验装置的不同之处是:这位同学采用了球形干燥管代替了长导管,并将干燥管的末端插入了饱和碳酸钠溶液中,在此处球形干燥管的作用除了使乙酸乙酯充分冷凝外还有防倒吸;加热一段时间后,可观察到烧杯D中液面上(填“上”或“下”)有无色油状液体生成,若分离该液体混合物,需要用到的玻璃仪器是分液漏斗,这种方法叫做分液.
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出乙醇(或CaCl2•6C2H5OH);再加入无水硫酸钠,然后进行蒸馏,收集产品乙酸乙酯时,温度应控制在77.1℃左右.
(4)乙酸可使紫色石蕊试液变红,说明乙酸具有酸性,写出乙酸与碳酸钠溶液反应的离子方程式2CH3COOH+CO32-=2CH3COO?+H2O+CO2↑.
 某化学兴趣设计实验制取乙酸乙酯.现用右图装置进行实验,在圆底烧瓶内加入碎瓷片,再加入由2ml 98%的浓H2SO4和3mL乙醇组成的混合液,通过分液漏斗向烧瓶内加入2mL醋酸,烧杯中加入饱和Na2CO3溶液.请回答下列问题:
某化学兴趣设计实验制取乙酸乙酯.现用右图装置进行实验,在圆底烧瓶内加入碎瓷片,再加入由2ml 98%的浓H2SO4和3mL乙醇组成的混合液,通过分液漏斗向烧瓶内加入2mL醋酸,烧杯中加入饱和Na2CO3溶液.请回答下列问题:已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH.
②有关有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点(℃) | 34.7 | 78.5 | 118 | 77.1 |
(2)与书中采用的实验装置的不同之处是:这位同学采用了球形干燥管代替了长导管,并将干燥管的末端插入了饱和碳酸钠溶液中,在此处球形干燥管的作用除了使乙酸乙酯充分冷凝外还有防倒吸;加热一段时间后,可观察到烧杯D中液面上(填“上”或“下”)有无色油状液体生成,若分离该液体混合物,需要用到的玻璃仪器是分液漏斗,这种方法叫做分液.
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出乙醇(或CaCl2•6C2H5OH);再加入无水硫酸钠,然后进行蒸馏,收集产品乙酸乙酯时,温度应控制在77.1℃左右.
(4)乙酸可使紫色石蕊试液变红,说明乙酸具有酸性,写出乙酸与碳酸钠溶液反应的离子方程式2CH3COOH+CO32-=2CH3COO?+H2O+CO2↑.
7.将22.4g铜锌合金均分为两份,向一份中加400mL一定浓度的稀硝酸,二者恰好完全反应,生成标准状况下的NO气体4.48L,若将另一份充分加热至质量恒重时,则生成的固体质量为( )
| A. | 32.0g | B. | 16.0 | C. | 18.0 | D. | 36.0 |
14.下列说法不能证明醋酸(CH3COOH)是弱电解质的是( )
| A. | 常温下0.1mol•L-1醋酸溶液稀释1000倍,测得pH约为5 | |
| B. | 用同浓度的NaOH溶液中和相同体积、相同pH的盐酸和醋酸溶液,比较消耗碱液体积的大小 | |
| C. | 醋酸钠溶液中加入酚酞试液后变红 | |
| D. | 0.01mol•L-1的CH3COOH溶液导电性实验中灯泡较暗 |
4.下列说法正确的是( )
| A. | 向鸡蛋清的溶液中加入浓的硫酸铵溶液,蛋白质的性质发生改变并凝聚 | |
| B. | 将牛油和烧碱溶液混合加热,充分反应后加入热的饱和食盐水,下层析出肥皂 | |
| C. | 油脂为髙分子化合物,分子结构中都含有酯基 | |
| D. | 纤维素、麦芽糖在一定条件下均可转化为葡萄糖 |
11.下列说法正确的是( )
| A. | 氯气和液氯是两种不同的物质 | |
| B. | NH3是电解质,所以氨水能导电 | |
| C. | 氨不能用浓硫酸干燥,但可以用无水CaCl2干燥 | |
| D. | 新制的氯水呈酸性,向其中滴加几滴紫色石蕊试液并振荡,溶液先变红后褪色 |
4.关于如图所示装置的说法错误的是( )


| A. | 该装置能将化学能转化成电能 | B. | 铜片周围溶液变为蓝色 | ||
| C. | 电子由锌片通过外电路流向铜片 | D. | 溶液中SO42-向负极方向流动 |
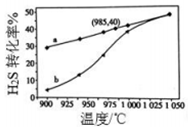 废气中的H2S通过高温热分解可制取氢气:2H2S(g)?2H2(g)+S2(g).在3L密闭容器中,控制不同温度进行H2S分解实验.
废气中的H2S通过高温热分解可制取氢气:2H2S(g)?2H2(g)+S2(g).在3L密闭容器中,控制不同温度进行H2S分解实验.