题目内容
11.下列说法正确的是( )| A. | 氯气和液氯是两种不同的物质 | |
| B. | NH3是电解质,所以氨水能导电 | |
| C. | 氨不能用浓硫酸干燥,但可以用无水CaCl2干燥 | |
| D. | 新制的氯水呈酸性,向其中滴加几滴紫色石蕊试液并振荡,溶液先变红后褪色 |
分析 A、氯气和液氯是两种状态不同组成相同的物质;
B、电解质必须是本身能电离而导电的化合物;
C、氨气为碱性气体应选用碱性干燥剂;
D、新制氯水含盐酸、HClO.
解答 解:A、氯气和液氯是两种状态不同组成相同的物质,是同一物质,而不是不同的物质,故A错误;
B、氨气本身不能电离出自由移动的离子,不属于电解质,故B错误;
C、氨气为碱性气体,与硫酸以及酸性氧化物都反应,不能用硫酸干燥,与CaCl2发生络合反应,也不能用CaCl2干燥,故C错误;
D、新制氯水含盐酸、HClO,则向其中滴加少量紫色石蕊试液,充分振荡后溶液先变红色后褪色,故D正确;
故选D.
点评 本题考查物质的性质,综合考查元素化合物知识,为高频考点,把握物质的性质及发生的化学反应为解答的关键,注意性质及反应中的现象分析,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.在一定体积的密闭容器中,进行如下化学反应:CH4(g)+H2O(g)?CO(g)+3H2(g),不同温度下达到平衡时,反应体系中各物质的浓度如表:
(1)该反应的平衡常数表达式为K=$\frac{{c}^{3}({H}_{2})c(CO)}{c(C{H}_{4})c({H}_{2}O)}$,正反应为吸热反应(填放热、吸热).
(2)能判断该反应是否已达到化学平衡状态的依据是ad
a.容器压强不变 b.c(CH4)=c(H2O)
c.v正(CH4)=v逆(H2) d.混合气体中c(CO)不变
氮化铝是共价键化合物,高碳热还原制备氮化铝的总反应化学方程式为(未配平):
Al2O3(s)+C(s)+N2(g)→AlN(s)+CO(g) …①
某氮化铝样品中含有氧化铝杂质.已知氮化铝和NaOH溶液能反应,并产生氨气,其反应方程式为:AlN+NaOH+H2O→NaAlO2+NH3↑…②,
氧化铝也能与氢氧化钠溶液反应而全部溶解…③
(3)配平化学化学方程式①:1Al2O3(s)+3C(s)+1N2(g)→2AlN(s)+3CO(g)
(4)反应②中产生气体的检验方法为湿润的红色石蕊试纸遇到气体变蓝;反应③的离子方程式Al2O3+2OH-=2AlO2-+H2O.
| 温度 | CH4(g) | H2O(g) | CO(g) | H2(g) |
| 500K | 0.8mol/L | 0.8mol/L | 0.2mol/L | 0.6mol/L |
| 800K | 0.6mol/L | 0.6mol/L | 0.4mol/L | 1.2mol/L |
| 1000K | 0.4mol/L | 0.4mol/L | 0.6mol/L | 1.8mol/L |
(2)能判断该反应是否已达到化学平衡状态的依据是ad
a.容器压强不变 b.c(CH4)=c(H2O)
c.v正(CH4)=v逆(H2) d.混合气体中c(CO)不变
氮化铝是共价键化合物,高碳热还原制备氮化铝的总反应化学方程式为(未配平):
Al2O3(s)+C(s)+N2(g)→AlN(s)+CO(g) …①
某氮化铝样品中含有氧化铝杂质.已知氮化铝和NaOH溶液能反应,并产生氨气,其反应方程式为:AlN+NaOH+H2O→NaAlO2+NH3↑…②,
氧化铝也能与氢氧化钠溶液反应而全部溶解…③
(3)配平化学化学方程式①:1Al2O3(s)+3C(s)+1N2(g)→2AlN(s)+3CO(g)
(4)反应②中产生气体的检验方法为湿润的红色石蕊试纸遇到气体变蓝;反应③的离子方程式Al2O3+2OH-=2AlO2-+H2O.
2.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 常温下,4gCH4中含有NA个C一H | |
| B. | 1molNa2O2固体中有含有离子总数为4NA | |
| C. | 100mol l8.4mol/L的浓硫酸与足量铜在加热条件下充分反应,转移电子1.84NA | |
| D. | l0gD2O中含有中子数4NA |
19.下列物质溶于水后,抑制了水的电离的是( )
| A. | Na2CO3 | B. | NH4Cl | C. | CH3COONa | D. | H2SO4 |
6.下列说法正确的是( )
| A. | Cu、Zn、H2SO4形成的原电池装置中,H2主要在Zn电极产生 | |
| B. | 往Fe和稀硫酸反应的装置中,加入少量CuSO4粉末,可加快产生H2的速率 | |
| C. | 2个氢原子变成1个氢气分子的过程中会放出一定的热量,是因为在相同条件下1个氢气分子具有的能量比2个氢原子的能量高 | |
| D. | 化学变化中伴随着化学键的断裂和形成,物理变化中一定没有化学键的断裂和形成 |
16.下列关于化学反应速率的说法正确的是( )
| A. | 1L0.1mol/L盐酸和1L0.1mol/L硫酸分别与1L2mol/LNaOH溶液反应的反应速率相同 | |
| B. | 化学反应速率为0.8mol/(L•s),其含义是时间为1s时,某物质的浓度是0.8mol/L | |
| C. | 等体积的0.1mol/L盐酸和0.1mol/L硝酸与形状和大小相同的大理石反应的速率相同 | |
| D. | 对于任何化学反应来说,反应速率越大,反应现象就越明显 |
3.下列说法正确的一组是( )
| A. | 不溶于水的盐(CaCO3、BaSO4等)都是弱电解质 | |
| B. | 0.5 mol•L-1的所有一元酸中氢离子浓度都是0.5 mol/L | |
| C. | 强酸溶液中氢离子浓度一定大于弱酸溶液中氢离子浓度 | |
| D. | 电解质溶液导电的原因是溶液中有自由移动的阴阳离子 |
15.下列表示物质结构的化学用语或模型正确的是( )
| A. | 含17个中子的镁元素的核素符号:${\;}_{17}^{29}$Mg | |
| B. | CH4分子的比例模型: | |
| C. | S2-离子的结构示意图: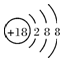 | |
| D. | HF的电子式: |
16.下列说法不正确的是( )
| A. | 氯化钠可用于制备纯碱 | |
| B. | 食品袋中常放有生石灰,能起到抗氧化剂的作用 | |
| C. | 大力发展新能源汽车能减少酸雨危害 | |
| D. | 石油裂化、煤的干馏、玉米制乙醇、蛋白质变性都属于化学变化 |