题目内容
8.化学与社会、生产和生活息息相关.下列说法错误的是( )| A. | 以Na2O2作供氧剂时,发生了氧化还原反应 | |
| B. | 在食品袋中放人CaCl2•6H2O,可防止食物受潮 | |
| C. | 人工合成食品级酯可以用作糖果的香料 | |
| D. | 用NH4Cl浓溶液除铁锈,因为NH4 Cl水解显酸性 |
分析 A.存在元素化合价的变化的反应是氧化还原反应;
B.无水氯化钙可以作吸水剂;
C.酯具有特殊的香味,可以做糖果的香料;
D.铁锈能与氢离子反应.
解答 解:A.以Na2O2作供氧剂时,Na2O2中O元素的化合价发生变化,所以发生了氧化还原反应,故A正确;
B.无水氯化钙可以作吸水剂,CaCl2•6H2O没有吸水性,不能作干燥剂,故B错误;
C.酯具有特殊的香味,对人体无害,所以人工合成食品级酯可以用作糖果的香料,故C正确;
D.铁锈能与氢离子反应,NH4Cl溶液显酸性,可除去铁锈,故D正确.
故选B.
点评 本题考查了化学知识在生产生活中的应用,题目难度不大,注意把握氧化还原反应的判断方法、干燥剂、盐的水解原理等知识点.

练习册系列答案
相关题目
18.下列操作会造成所配溶液的浓度偏低是的( )
| A. | 用烧杯盛氢氧化钠称量 | |
| B. | 浓硫酸溶解后立即转移到容量瓶内 | |
| C. | 用量筒量硫酸时俯视刻度 | |
| D. | 用量筒量硫酸时,倾倒后量筒没有洗涤 |
19.下列化学用语的描述不正确的是( )
| A. | 烧碱的分子式为NaOH | |
| B. | 中子数为15的硅原子:${\;}_{14}^{20}$Si | |
| C. | 乙醇的结构简式:C2H5OH | |
| D. | NH3•H2O的电离方程式:NH3•H2O?NH4++OH- |
16.高炉煤气为炼铁过程中产生的副产品,主要成分为N2、CO、CO2、H2O等,其中可燃成分CO含量约占25%左右,CO2、N2的含量分别占15%、55%.回答下列问题:
(1)上述提及的气体分子中,电子数相等的两种气体是N2、CO(写化学式).
(2)高炉煤气中CO具有较高的利用价值,可以与H2合成甲烷,已知有关反应的热化学方程式如下:
①H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ/mol
②CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283.0kJ/mol
③CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ/mol
则CO(g)+2H2(g)=CH4(g)+$\frac{1}{2}$O2(g)△H=+35.7kJ/mol.
(3)高炉煤气中N2的含量较高,利用CO前需要对CO 进行富集,实现CO和N2的分离.
①工业上常采用醋酸亚铜氨溶液来吸收CO,该反应的热化学方程式CH3COOCu(NH3)2(aq)+CO(g)═CH3COOCu(NH3)2•CO(aq)△H<0.吸收CO后的溶液经过适当处理可恢复为醋酸亚铜氨溶液,从而实现CO与吸收液的分离,分离过程可采取的措施有升温或减压(写出一种即可).
②到目前为止,CO吸附剂的开发大多数以亚铜为活性组分负载在各种载体上,然后采用变压吸附(PSA)方式在含N2体系中脱出CO.图是变压吸附回收高炉煤气中CO的流程图:

PSA-I吸附CO2时间对PSA-II中CO回收率的影响见下图,由此可见,为了保证载体亚铜吸附剂对CO的吸附和提纯要求,应采取的措施是尽量在PSA-I中将CO2脱除(保证PSA-I吸附CO2的时间),“放空气体”的主要成分为氮气.
(4)高炉炼铁过程中发生的主要反应为Fe2O3(s)+3CO(g)═2Fe (s)+3CO2(g).该反应在不同温度下的平衡常数如表所示:
①该反应的△H<0(填“>““<”或“=“).
②欲提高上述反应中CO 的转化率,可采取的措施是ab.
a.适当降低反应体系的温度
b.及时移出体系中的CO
c.加入合适的催化剂
d.减小容器的容积
e.增大Fe2O3的量.
(1)上述提及的气体分子中,电子数相等的两种气体是N2、CO(写化学式).
(2)高炉煤气中CO具有较高的利用价值,可以与H2合成甲烷,已知有关反应的热化学方程式如下:
①H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ/mol
②CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283.0kJ/mol
③CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ/mol
则CO(g)+2H2(g)=CH4(g)+$\frac{1}{2}$O2(g)△H=+35.7kJ/mol.
(3)高炉煤气中N2的含量较高,利用CO前需要对CO 进行富集,实现CO和N2的分离.
①工业上常采用醋酸亚铜氨溶液来吸收CO,该反应的热化学方程式CH3COOCu(NH3)2(aq)+CO(g)═CH3COOCu(NH3)2•CO(aq)△H<0.吸收CO后的溶液经过适当处理可恢复为醋酸亚铜氨溶液,从而实现CO与吸收液的分离,分离过程可采取的措施有升温或减压(写出一种即可).
②到目前为止,CO吸附剂的开发大多数以亚铜为活性组分负载在各种载体上,然后采用变压吸附(PSA)方式在含N2体系中脱出CO.图是变压吸附回收高炉煤气中CO的流程图:

PSA-I吸附CO2时间对PSA-II中CO回收率的影响见下图,由此可见,为了保证载体亚铜吸附剂对CO的吸附和提纯要求,应采取的措施是尽量在PSA-I中将CO2脱除(保证PSA-I吸附CO2的时间),“放空气体”的主要成分为氮气.

(4)高炉炼铁过程中发生的主要反应为Fe2O3(s)+3CO(g)═2Fe (s)+3CO2(g).该反应在不同温度下的平衡常数如表所示:
| 温度/℃ | 1000 | 1115 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
②欲提高上述反应中CO 的转化率,可采取的措施是ab.
a.适当降低反应体系的温度
b.及时移出体系中的CO
c.加入合适的催化剂
d.减小容器的容积
e.增大Fe2O3的量.
3.某溶液中含K+、Fe3+、Fe2+、Cl-、CO32-、NO3-、SO42-、SiO32-、I-中的若干种,某同学欲探究该溶液的组成,
进行如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰.
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成.
Ⅲ.取Ⅱ反应后的溶液分别置于两支试管中,第一支试管中加入BaCl2溶液,有白色沉淀生成,再滴加KSCN溶液,上层清液变红;第二支试管中加入CCl4,充分振荡静置后溶液分层,下层为无色.下列说法正确的是( )
进行如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰.
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成.
Ⅲ.取Ⅱ反应后的溶液分别置于两支试管中,第一支试管中加入BaCl2溶液,有白色沉淀生成,再滴加KSCN溶液,上层清液变红;第二支试管中加入CCl4,充分振荡静置后溶液分层,下层为无色.下列说法正确的是( )
| A. | 原溶液中肯定不含Fe2+、NO3-、SiO32-、I- | |
| B. | 为确定是否含有Cl-,可取原溶液加入过量硝酸银溶液,观察是否产生白色沉淀 | |
| C. | 步骤Ⅱ中无色气体是NO气体 | |
| D. | 原溶液中肯定含有K+、Fe2+、NO3-、SO42- |
13.实验测得pH=1.0的某溶液中还可能大量存在:Na+、Fe2+、Al3+、NH4+、SO42-、Cl-中的若干种离子,现进行了如下实验:
步骤I,取该溶液10.0mL,加入过量1.0mol/L Ba(NO3)2溶液,产生白色沉淀A和无色气体B,B遇空气立即变为红棕色;
步骤Ⅱ.向I所得的溶液中加入过量1.0mol/L NaOH溶液,有红褐色沉淀C和无色刺激性气体D生成.用铂丝蘸取所得溶液,在火焰上灼烧,火焰呈黄色;
步骤Ⅲ.向Ⅱ所得的溶液中通入过量CO2有沉淀E生成.
下列推断错误的是( )
步骤I,取该溶液10.0mL,加入过量1.0mol/L Ba(NO3)2溶液,产生白色沉淀A和无色气体B,B遇空气立即变为红棕色;
步骤Ⅱ.向I所得的溶液中加入过量1.0mol/L NaOH溶液,有红褐色沉淀C和无色刺激性气体D生成.用铂丝蘸取所得溶液,在火焰上灼烧,火焰呈黄色;
步骤Ⅲ.向Ⅱ所得的溶液中通入过量CO2有沉淀E生成.
下列推断错误的是( )
| A. | 步骤I中白色沉淀A的化学式为BaSO4 | |
| B. | 步骤Ⅱ中产生沉淀C的反应:Fe3++3OH-=Fe(OH)3↓ | |
| C. | 原溶液一定含有:Na+、Fe2+、Al3+、SO42- | |
| D. | CO2先后分别与NaOH(aq)、NaAlO2( aq)反应 |
20.下列关于有机物的说法正确的是( )
| A. | 分子式为C5H11Cl的有机物有8种同分异构体 | |
| B. | 塑料的老化是因为其主要成分在空气中发生了缓慢的加成反应 | |
| C. | 乙醇和乙酸都能与碳酸氢钠溶液反应 | |
| D. | 富含糖类和蛋白质的物质都易被人体消化 |
8.氨的合成是最重要的化工生产之一.
Ⅰ.工业上合成氨用的H2有多种制取的方法:
①用焦炭跟水反应:C(s)+H2O(g)$\frac{\underline{\;高温\;}}{\;}$ CO(g)+H2(g);
②用天然气跟水蒸气反应:CH4(g)+H2O(g) $\frac{\underline{\;催化剂\;}}{高温}$ CO(g)+3H2(g)
已知有关反应的能量变化如图,且方法②的反应只能在高温下发生,则方法②中反应的△H=a+3b-c kJ/moL.

Ⅱ.在3个1L的密闭容器中,同温度下、使用相同催化剂分别进行反应:3H2(g)+N2(g) $?_{催化剂}^{高温、高压}$2NH3(g),按不同方式投入反应物,保持恒温、恒容,反应达到平衡时有关数据为:
(1)下列能说明该反应已达到平衡状态的是
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v(N2)正=3v(H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变
(2)甲容器中达到平衡所需要的时间t>5min (填>、<或=)
(3)乙中从反应开始到平衡时N2的平均反应速率0.2mol•L-1•min-1(注明单位).
(4)分析上表数据,下列关系正确的是c.
a.2c1=3mol/L b.ω1=ω2 c. 2ρ1=ρ2
(5)该温度下,容器乙中,该反应的平衡常数K=$\frac{4}{81}$(用分数表示)(mol/L)-2.
(6)常温下NH4+(aq)+H2O(l)?NH3•H2O(aq)+H+(aq)的化学平衡常数为5.55×10-10 mol•L-1,则NH3•H2O的电离平衡常数K=1.80×10-5mol•L-1(保留三位有效数字).已知草酸的电离常数为:Ka1=5.9×10-2 Ka2=6.4×10-5,则草酸氢铵的水溶液中离子浓度由大到小的顺序是:c(NH4+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-).
Ⅲ.(1)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图1所示.
电池正极的电极反应式是N2+6e-+8H+=2NH4+,A是NH4Cl.
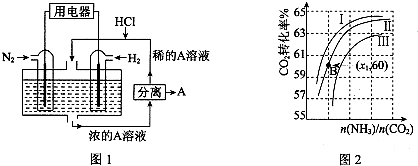
(2)用氨合成尿素的反应为2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g).工业生产时,原料气带有水蒸气.图2表示CO2的转化率与氨碳比$\frac{n(N{H}_{3})}{n(C{O}_{2})}$、水碳比$\frac{n({H}_{2}O)}{n(C{O}_{2})}$的变化关系.
①曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是Ⅲ.
②测得B点氨的转化率为40%,则x13.
Ⅰ.工业上合成氨用的H2有多种制取的方法:
①用焦炭跟水反应:C(s)+H2O(g)$\frac{\underline{\;高温\;}}{\;}$ CO(g)+H2(g);
②用天然气跟水蒸气反应:CH4(g)+H2O(g) $\frac{\underline{\;催化剂\;}}{高温}$ CO(g)+3H2(g)
已知有关反应的能量变化如图,且方法②的反应只能在高温下发生,则方法②中反应的△H=a+3b-c kJ/moL.

Ⅱ.在3个1L的密闭容器中,同温度下、使用相同催化剂分别进行反应:3H2(g)+N2(g) $?_{催化剂}^{高温、高压}$2NH3(g),按不同方式投入反应物,保持恒温、恒容,反应达到平衡时有关数据为:
| 容 器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3mol H2、2mol N2 | 6mol H2、4mol N2 | 2mol NH3 |
| 达到平衡的时间(min) | t | 5 | 8 |
| 平衡时N2的浓度(mol•L-1) | c1 | 3 | |
| N2的体积分数 | ω1 | ω2 | ω3 |
| 混合气体密度(g•L-1) | ρ1 | ρ2 |
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.v(N2)正=3v(H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变
(2)甲容器中达到平衡所需要的时间t>5min (填>、<或=)
(3)乙中从反应开始到平衡时N2的平均反应速率0.2mol•L-1•min-1(注明单位).
(4)分析上表数据,下列关系正确的是c.
a.2c1=3mol/L b.ω1=ω2 c. 2ρ1=ρ2
(5)该温度下,容器乙中,该反应的平衡常数K=$\frac{4}{81}$(用分数表示)(mol/L)-2.
(6)常温下NH4+(aq)+H2O(l)?NH3•H2O(aq)+H+(aq)的化学平衡常数为5.55×10-10 mol•L-1,则NH3•H2O的电离平衡常数K=1.80×10-5mol•L-1(保留三位有效数字).已知草酸的电离常数为:Ka1=5.9×10-2 Ka2=6.4×10-5,则草酸氢铵的水溶液中离子浓度由大到小的顺序是:c(NH4+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-).
Ⅲ.(1)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图1所示.
电池正极的电极反应式是N2+6e-+8H+=2NH4+,A是NH4Cl.

(2)用氨合成尿素的反应为2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g).工业生产时,原料气带有水蒸气.图2表示CO2的转化率与氨碳比$\frac{n(N{H}_{3})}{n(C{O}_{2})}$、水碳比$\frac{n({H}_{2}O)}{n(C{O}_{2})}$的变化关系.
①曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是Ⅲ.
②测得B点氨的转化率为40%,则x13.
9.下列反应中,光照对反应几乎没有影响的是( )
| A. | 次氯酸分解 | B. | 甲烷与氯气反应 | C. | 甲烷与氧气反应 | D. | 氯气与氢气反应 |