题目内容
9.NA代表阿伏加德罗常数的值.下列叙述正确的是( )| A. | 常温常压下,2.24 LSO2中所含氧原子数为0.2NA | |
| B. | 将1 mol Cl2通入水中,HC1O、Cl-、ClO-粒子数之和为2NA | |
| C. | 1 mol NO2与足量H2O反应,转移的电子数为NA | |
| D. | 0.1 mol熔融的NaHSO4中阳离子数目为0.lNA |
分析 A、常温常压下,气体摩尔体积大于22.4L/mol;
B、氯气和水反应是可逆反应;
C、二氧化氮和水的反应中,3mol二氧化氮转移2mol电子;
D、硫酸氢钠在熔融状态下电离为钠离子和硫酸氢根离子.
解答 解:A、常温常压下,气体摩尔体积大于22.4L/mol,故2.24L二氧化硫的物质的量小于0.1mol,故含有的原子个数小于0.2NA个,故A错误;
B、氯气和水反应是可逆反应,在氯水中含氯气分子、HCl和HClO,故溶液中的N(HC1O)+N(Cl-)+N(ClO-)+2N(Cl2)=2NA,故B错误;
C、二氧化氮和水的反应中,3mol二氧化氮转移2mol电子,故1mol二氧化氮转移$\frac{2}{3}$NA个电子,故C错误;
D、硫酸氢钠在熔融状态下电离为钠离子和硫酸氢根离子,故0.1mol硫酸氢钠中含0.1NA个阳离子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
19.标准状况下,同体积的下列物质中所含有的分子数最多的是( )
| A. | CO2 | B. | H2 | C. | H2O | D. | O2 |
20.下列有关说法正确的是( )
| A. | 甲烷是天然气的主要成分,能发生取代反应,但不能发生氧化反应 | |
| B. | 实验室中,可用金属钠检验乙醇中是否含有水 | |
| C. | 只用水无法鉴别苯、乙酸和四氯化碳 | |
| D. | 植物油不能用于萃取溴水中的溴 |
17.化学与生产、生活密切相关.下列叙述正确的是( )
| A. | 我国古代四大发明之一黑火药由硫酸、硝酸和木炭按一定比例混合制成 | |
| B. | PH计不能用于酸碱中和滴定终点的判断 | |
| C. | 石油的分馏,煤的干馏、气化、液化均是物理变化 | |
| D. | 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 |
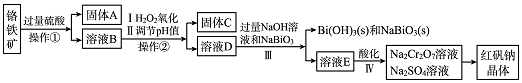
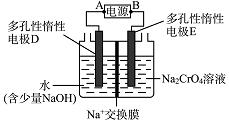
4.教材中给出了Na2O2与水反应的化学方程式,某学习小组通过实验研究Na2O2与水发反应机理
(1)Na2O2的电子式为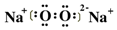 ,很明显,实验证实了溶液a中H2O2的存在,应用同位素示踪原理可以表
,很明显,实验证实了溶液a中H2O2的存在,应用同位素示踪原理可以表
示反应的机理,写出Na218O2与H2O反应的化学方程式2Na218O2+2H2O═2Na18OH+2NaOH+18O2↑.
(2)操作Ⅱ中红色褪去的可能原因是溶液a中过量H2O2与酚酞发生反应.
(3)用反应2MnO4-+5H2O2+6H+=2Mn2++502↑+8H2O测定溶液a中H2O2含量.取20.00mL溶液a,用稀H2SO4(填化学式)酸化,用0.002mol•L-1KMnO4溶液滴定,至终点时平均消耗10.00mLKMnO4溶液.滴定时KMnO4溶液应装在酸(填酸或碱)式滴定管中,终点确定的方法是滴至最后一滴时溶液由紫色变为无色,且半分钟内不变色,经计算溶液a中c(H2O2)=0.0025mol•L-1
(4)向溶液a中滴加FeSO4溶液,发生反应的离子方程式为4H2O2+4Fe2++6H2O=O2↑+4Fe(OH)3↓+8Na+.
(5)向FeSO4溶液中加入一定量Na202固体,并以物质的量为2:1发生反应,反应中无气体生成,写出
反应的离子方程式3Na2O2+6 Fe2++6H2O=6Na++4Fe(OH)3↓+2Fe3+.
| 操作 | 现象 |
| Ⅰ.向盛有4.0gNa2O2的烧杯中加入50mL蒸馏水 | 剧烈反应,产生的气体能使带火星木条复燃,固体全部溶解后,得到的无色溶液a |
| Ⅱ.向溶液a中滴入两滴酚酞 | 溶液变红,10分钟后溶液颜色明显变浅,稍后,溶液变为无色 |
| Ⅲ.向溶液中加入少量MnO2粉末 | 又有大量气泡产生,产生的气体也能使带火星木条复燃 |
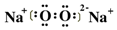 ,很明显,实验证实了溶液a中H2O2的存在,应用同位素示踪原理可以表
,很明显,实验证实了溶液a中H2O2的存在,应用同位素示踪原理可以表示反应的机理,写出Na218O2与H2O反应的化学方程式2Na218O2+2H2O═2Na18OH+2NaOH+18O2↑.
(2)操作Ⅱ中红色褪去的可能原因是溶液a中过量H2O2与酚酞发生反应.
(3)用反应2MnO4-+5H2O2+6H+=2Mn2++502↑+8H2O测定溶液a中H2O2含量.取20.00mL溶液a,用稀H2SO4(填化学式)酸化,用0.002mol•L-1KMnO4溶液滴定,至终点时平均消耗10.00mLKMnO4溶液.滴定时KMnO4溶液应装在酸(填酸或碱)式滴定管中,终点确定的方法是滴至最后一滴时溶液由紫色变为无色,且半分钟内不变色,经计算溶液a中c(H2O2)=0.0025mol•L-1
(4)向溶液a中滴加FeSO4溶液,发生反应的离子方程式为4H2O2+4Fe2++6H2O=O2↑+4Fe(OH)3↓+8Na+.
(5)向FeSO4溶液中加入一定量Na202固体,并以物质的量为2:1发生反应,反应中无气体生成,写出
反应的离子方程式3Na2O2+6 Fe2++6H2O=6Na++4Fe(OH)3↓+2Fe3+.
1.用NA表示阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 78g苯中含有的碳碳双键的数目为3NA | |
| B. | 16g由Cu2S和CuO组成的混合物中含有的阳离子数为0.2NA | |
| C. | 将1molH2与1molI2充入一密闭容器中充分反应后,转移的电子数为2NA | |
| D. | 1mo1Fe与足量的浓硫酸共热反应,生成SO2的分子数为NA |
9.甲醇是重要的化工原料,又是一种可再生能源,具有广泛的开发和应用前景.
(1)已知反应CO(g)+2H2(g)═CH3OH(g)△H=-99kJ.mol-1中的相关化学键键能如表:
则x=1076.
(2)在一容积可变的密闭容器中,1molCO与2molH2发生反应:
CO(g)+2H2(g)$\stackrel{催化剂}{?}$CH3OH(g)△H1<0,
CO在不同温度下的平衡转化率(α)与压强的关系如图1所示.

①a、b两点的反应速率:v(a)<v(b)(填“>”、“<”、“=”)
②T1<T2 (填“>”、“<”、“=”),原因是该反应是放热反应,温度升高,平衡逆向移动,CO的平衡转化率减小,故Tl<T2
③在c点条件下,下列叙述能说明上述反应能达到化学平衡状态的是bc(填代号)
a.H2的消耗速率是CH3OH生成速率的2倍 b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变 d.CO和CH3OH的物质的量之和保持不变
④计算图中a点的平衡常数KP=1.6×10-7(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(3)利用合成气(主要成分为CO、CO2和H2)合成甲醇,发生主要反应如下:
I:CO(g)+2H2(g)$\stackrel{催化剂}{?}$CH3OH(g)△H1
Ⅱ:CO2(g)+H2(g)$\stackrel{催化剂}{?}$CO(g)+H2O(g)△H2
Ⅲ:CO2(g)+3H2(g)$\stackrel{催化剂}{?}$CH3OH(g)+H2O(g)△H3
上述反应对应的平衡常数分别为K1、K2、K3,它们随温度变化曲线如图2所示.则△H1<△H3(填“>”、“<”、“=”),理由是由图可知,随着温度升高,K2减小,则△H2>0,根据盖斯定律又得△H3=△H1+△H2,所以△H1<△H3.
(1)已知反应CO(g)+2H2(g)═CH3OH(g)△H=-99kJ.mol-1中的相关化学键键能如表:
| 化学键 | H-H | C-O | C≡C | H-O | C-H |
| E/(KJ.mol-1) | 436 | 343 | x | 465 | 413 |
(2)在一容积可变的密闭容器中,1molCO与2molH2发生反应:
CO(g)+2H2(g)$\stackrel{催化剂}{?}$CH3OH(g)△H1<0,
CO在不同温度下的平衡转化率(α)与压强的关系如图1所示.

①a、b两点的反应速率:v(a)<v(b)(填“>”、“<”、“=”)
②T1<T2 (填“>”、“<”、“=”),原因是该反应是放热反应,温度升高,平衡逆向移动,CO的平衡转化率减小,故Tl<T2
③在c点条件下,下列叙述能说明上述反应能达到化学平衡状态的是bc(填代号)
a.H2的消耗速率是CH3OH生成速率的2倍 b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变 d.CO和CH3OH的物质的量之和保持不变
④计算图中a点的平衡常数KP=1.6×10-7(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(3)利用合成气(主要成分为CO、CO2和H2)合成甲醇,发生主要反应如下:
I:CO(g)+2H2(g)$\stackrel{催化剂}{?}$CH3OH(g)△H1
Ⅱ:CO2(g)+H2(g)$\stackrel{催化剂}{?}$CO(g)+H2O(g)△H2
Ⅲ:CO2(g)+3H2(g)$\stackrel{催化剂}{?}$CH3OH(g)+H2O(g)△H3
上述反应对应的平衡常数分别为K1、K2、K3,它们随温度变化曲线如图2所示.则△H1<△H3(填“>”、“<”、“=”),理由是由图可知,随着温度升高,K2减小,则△H2>0,根据盖斯定律又得△H3=△H1+△H2,所以△H1<△H3.
10.下列叙述正确的是( )
| A. | 非金属原子间以共价键结合的物质一定是共价化合物 | |
| B. | 含有共价键的化合物一定是共价化合物 | |
| C. | 凡是能电离出离子的化合物一定是离子化合物 | |
| D. | 凡是含有离子键的化合物一定是离子化合物 |