题目内容
19.下列有关化学用语使用正确的是( )| A. | 硫原子的原子结构示意图: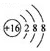 | |
| B. | 原子核内有10个质子的氧原子${\;}_{8}^{18}$O | |
| C. | NH4Cl的电子式: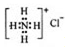 | |
| D. | 邻氯甲苯的结构简式: |
分析 A.硫原子原子核外有16个电子最外层6个电子;
B.原子核内有10个中子的氧原子;
C.电子式需要标注原子的最外层电子,氯离子最外层电子未标注;
D.甲苯中甲基邻位上有氯原子.
解答 解:A.硫原子原子核外有16个电子最外层6个电子 ,故A错误;
,故A错误;
B.${\;}_{8}^{18}$O原子核内有8个质子,10个中子的氧原子,故B错误;
C.氯化铵是离子化合物,由氨根离子与氯离子构成,电子式为: ,故C错误;
,故C错误;
D.邻氯甲苯是甲苯中甲基邻位上有氯原子,物质的结构简式: ,故D正确;
,故D正确;
故选D.
点评 本题考查常用化学用语,准确判断物质所含化学键类型、熟练掌握电子式书写方法即可解答,题目难度不大.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
11. 研究表明丰富的CO2完全可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)到本世纪中叶将枯竭的危机,同时又可缓解由CO2累积所产生的温室效应,实现CO2的良性循环.
研究表明丰富的CO2完全可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)到本世纪中叶将枯竭的危机,同时又可缓解由CO2累积所产生的温室效应,实现CO2的良性循环.
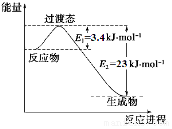
(1)目前工业上有一种方法是用CO2和H2在230℃催化剂条件下转化生成甲醇蒸汽和水蒸气.图表示恒压容器中0.5mol CO2和1.5mol H2转化率达80%时的能量变化示意图.
①写出该反应的热化学方程式:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49 kJ•mol-1.
②能判断该反应达到化学平衡状态的依据是bd.
a.容器中压强不变
b.H2的体积分数不变
c.c(H2)=3c(CH3OH)
d.容器中密度不变
e.2个C=O断裂的同时有6个H-H断裂.
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如表三组数据:
①在实验2条件下平衡常数K=0.17
②在实验3中,若平衡时CO转化率大于水蒸气转化率,则a/b 的值0<$\frac{a}{b}$<1(填具体值或范围).
③在实验4中,若保持990℃,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时V正<V逆(填“>”、“=”或“<”)
(3)已知在常温下,甲醇是优质的清洁燃料,可制作燃料电池.
①已知:①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H1=-1275.6kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H2=-566.0kJ•mol-1
③H2O(g)═H2O(l)△H3=-44.0kJ•mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ/mol.
(4)已知草酸是一种二元酸,草酸氢钠溶液显酸性.常温下向10Ml0.01mol/LH2C2O4溶液中滴加10mL0.01mol/LNaOH溶液时,比较溶液中各种离子浓度大小关系c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-)
(5)以甲醚空气氢氧化钾溶液为原料,石墨为电极可构成燃料电池,该电池的负极反应式为CH3OCH3+16OH--12e-=2CO32-+11H2O.
 研究表明丰富的CO2完全可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)到本世纪中叶将枯竭的危机,同时又可缓解由CO2累积所产生的温室效应,实现CO2的良性循环.
研究表明丰富的CO2完全可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)到本世纪中叶将枯竭的危机,同时又可缓解由CO2累积所产生的温室效应,实现CO2的良性循环.(1)目前工业上有一种方法是用CO2和H2在230℃催化剂条件下转化生成甲醇蒸汽和水蒸气.图表示恒压容器中0.5mol CO2和1.5mol H2转化率达80%时的能量变化示意图.
①写出该反应的热化学方程式:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49 kJ•mol-1.
②能判断该反应达到化学平衡状态的依据是bd.
a.容器中压强不变
b.H2的体积分数不变
c.c(H2)=3c(CH3OH)
d.容器中密度不变
e.2个C=O断裂的同时有6个H-H断裂.
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如表三组数据:
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需 时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
②在实验3中,若平衡时CO转化率大于水蒸气转化率,则a/b 的值0<$\frac{a}{b}$<1(填具体值或范围).
③在实验4中,若保持990℃,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时V正<V逆(填“>”、“=”或“<”)
(3)已知在常温下,甲醇是优质的清洁燃料,可制作燃料电池.
①已知:①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H1=-1275.6kJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H2=-566.0kJ•mol-1
③H2O(g)═H2O(l)△H3=-44.0kJ•mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H=-442.8kJ/mol.
(4)已知草酸是一种二元酸,草酸氢钠溶液显酸性.常温下向10Ml0.01mol/LH2C2O4溶液中滴加10mL0.01mol/LNaOH溶液时,比较溶液中各种离子浓度大小关系c(Na+)>c(HC2O4-)>c(H+)>c(C2O42-)>c(OH-)
(5)以甲醚空气氢氧化钾溶液为原料,石墨为电极可构成燃料电池,该电池的负极反应式为CH3OCH3+16OH--12e-=2CO32-+11H2O.
4.下列实验装置不能达到实验目的是( )

| A. | 比较非金属性强弱:Si弱于C,C弱于S | |
| B. | 用四氯化碳提取碘水中的碘单质 | |
| C. | 观察烧碱的焰色反应 | |
| D. | 比较NaHCO3和Na2CO3的热稳定性 |
11.化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A. | 氢氧燃料电池在碱性介质中的负极反应式:O2+2H2O+4e-=4OH- | |
| B. | 电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-=Cl2↑ | |
| C. | 粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ | |
| D. | 钢铁发生电化学腐蚀的正极反应式:Fe-2e-=Fe2+ |
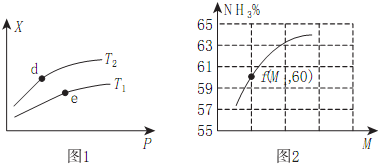 已知有关热化学方程式为:①4NH3(g)+5O2(g)4NO(g)+6H2O(g)△H=-905kJ/mol;②3H2(g)+N2(g)2NH3(g)△H=-92.4kJ/mol;③2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol;④N2(g)+O2(g)=2NO(g)△H=QkJ/mol;反应①中有关化学键的键能(kJ/mol)如下:H-O:463,H-N:391,O=O:497
已知有关热化学方程式为:①4NH3(g)+5O2(g)4NO(g)+6H2O(g)△H=-905kJ/mol;②3H2(g)+N2(g)2NH3(g)△H=-92.4kJ/mol;③2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol;④N2(g)+O2(g)=2NO(g)△H=QkJ/mol;反应①中有关化学键的键能(kJ/mol)如下:H-O:463,H-N:391,O=O:497