��Ŀ����
11��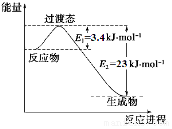 �о������ḻ��CO2��ȫ������Ϊ��̼Դ�������ǰӦ����㷺��̼Դ��ʯ�ͺ���Ȼ��������������Ҷ���ݽߵ�Σ����ͬʱ�ֿɻ�����CO2�ۻ�������������ЧӦ��ʵ��CO2������ѭ����
�о������ḻ��CO2��ȫ������Ϊ��̼Դ�������ǰӦ����㷺��̼Դ��ʯ�ͺ���Ȼ��������������Ҷ���ݽߵ�Σ����ͬʱ�ֿɻ�����CO2�ۻ�������������ЧӦ��ʵ��CO2������ѭ������1��Ŀǰ��ҵ����һ�ַ�������CO2��H2��230�����������ת�����ɼ״�������ˮ������ͼ��ʾ��ѹ������0.5mol CO2��1.5mol H2ת���ʴ�80%ʱ�������仯ʾ��ͼ��
��д���÷�Ӧ���Ȼ�ѧ����ʽ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49 kJ•mol-1��
�����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������bd��
a��������ѹǿ����
b��H2�������������
c��c��H2��=3c��CH3OH��
d���������ܶȲ���
e��2��C=O���ѵ�ͬʱ��6��H-H���ѣ�
��2������ͬ����CO��g����H2O��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У����з�ӦCO��g��+H2O��g��?CO2��g��+H2��g�����õ�����������ݣ�
| ʵ���� | �¶ȡ� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
����ʵ��3�У���ƽ��ʱCOת���ʴ���ˮ����ת���ʣ���a/b ��ֵ0��$\frac{a}{b}$��1�������ֵ��Χ����
����ʵ��4�У�������990�棬�ڴ������м���CO��H2O��CO2��H2��Ϊ1mol�����ʱV����V�������������=��������
��3����֪�ڳ����£��״������ʵ����ȼ�ϣ�������ȼ�ϵ�أ�
����֪����2CH3OH��l��+3O2��g���T2CO2��g��+4H2O��g����H1=-1275.6kJ•mol-1
��2CO��g��+O2��g���T2CO2��g����H2=-566.0kJ•mol-1
��H2O��g���TH2O��l����H3=-44.0kJ•mol-1
д���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽCH3OH��l��+O2��g��=CO��g��+2H2O��l����H=-442.8kJ/mol��
��4����֪������һ�ֶ�Ԫ�ᣬ����������Һ�����ԣ���������10Ml0.01mol/LH2C2O4��Һ�еμ�10mL0.01mol/LNaOH��Һʱ���Ƚ���Һ�и�������Ũ�ȴ�С��ϵc��Na+����c��HC2O4-����c��H+����c��C2O42-����c��OH-��
��5���Լ��ѿ�������������ҺΪԭ�ϣ�ʯīΪ�缫�ɹ���ȼ�ϵ�أ��õ�صĸ�����ӦʽΪCH3OCH3+16OH--12e-=2CO32-+11H2O��
���� ��1���ٷ�����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g��������ͼ1��֪��0.5mol CO2��1.5mol H2ת���ʴ�80%ʱ����23kJ-3.4kJ=19.6kJ������1mol������̼�����ų�������ȷ����H����д�÷�Ӧ���Ȼ�ѧ����ʽ��
�ڵ���Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�ȡ��ٷֺ������䣬�Լ��ɴ�������һЩ��Ҳ�������仯��ע��ѡ���жϵ���������Ӧ���ŷ�Ӧ�Ľ��з����仯�������������ɱ仯����ֵʱ��˵�����淴Ӧ����ƽ��״̬��
��2��������ͼ��������ʽ����ƽ��Ũ�ȣ��ٸ���ƽ�ⳣ�������������Ũ����֮�����Է�Ӧ���Ũ����֮�����м��㣻
���ڷ�Ӧ�е���Ӧ������ʵ���֮�ȵ��ڻ�ѧ������֮��ʱ������Ӧ���ת������ȣ�ijһ�ַ�Ӧ��Խ�࣬��ת����Խ�ͣ�����һ�ַ�Ӧ���ת������Խ�ߣ��ݴ˴��⣻
�۸���Ũ����Qc��ƽ�ⳣ��K�Ĵ�С���жϷ�Ӧ���еķ�����ȷ�����淴Ӧ�����ʵĴ�С��ϵ��
��3�����ݸ�˹���ɽ��м��㣬��$\frac{��-��+�ۡ�4}{2}$�ó���ȷ���ۣ�
��4��H2C2O4��NaOH��Ӧ����NaHC2O4��NaHC2O4��Һ������˵����Һ�е������ˮ�⣬���˱Ƚ���Һ��HC2O4-��C2O42-��H2C2O4��H+��Ũ�ȴӴ�С��˳��
��5��ԭ��ظ�������������Ӧ�������ڸ����ŵ磬��������������̼�����ˮ��������д�缫��Ӧʽ��
��� �⣺��1���ٸ���ͼ1��֪��0.5mol CO2��1.5mol H2ת���ʴ�80%ʱ����23kJ-3.4kJ=19.6kJ��1mol������̼��Ӧ�ų�������Ϊ$\frac{1mol}{0.5mol��80%}$��19.6kJ=49kJ����÷�Ӧ���Ȼ�ѧ����ʽ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49kJ•mol-1��
�ʴ�Ϊ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����H=-49 kJ•mol-1��
��a����Ӧ�ٺ�ѹ�����н��У���������ѹǿ���䣬����˵����Ӧ�ﵽƽ��״̬����a����
b��H2������������䣬˵����Ӧ�ﵽƽ��״̬����b��ȷ��
c��ƽ��ʱ�����ʵ�Ũ��֮��ȡ�������ʵ���ʼ���ʵ�����ת���ʣ���c��H2��=3c��CH3OH��������˵����Ӧ�ﵽƽ��״̬����c����
d���ܶȦ�=$\frac{m}{V}$����������䣬�����䣬���������ܶȲ��䣬˵����Ӧ�ﵽƽ��״̬����d��ȷ��
e��2��C=O����������Ӧ��ͬʱ��6��H-H����Ҳ������Ӧ���ʲ���˵����Ӧ�ﵽƽ��״̬����e����
�ʴ�Ϊ��bd��
��2����H2O��g��+CO��g��?CO2��g��+H2��g��
��ʼŨ�� 0.5mol/L 1mol/L 0 0
ת��Ũ�� 0.2mol/L 0.2mol/l 0.2mol/l 0.2mol/l
ƽ��Ũ�� 0.3mol/L 0.8mol/L 0.2mol/l 0.2mol/l
K=$\frac{c��C{O}_{2}��•c��{H}_{2}��}{c��CO��•c��{H}_{2}O��}$=$\frac{0.2��0.2}{0.3��0.8}$=0.17��
�ʴ�Ϊ��0.17��
���ڷ�Ӧ�е���Ӧ������ʵ���֮�ȵ��ڻ�ѧ������֮��ʱ������Ӧ���ת������ȣ�ijһ�ַ�Ӧ��Խ�࣬��ת����Խ�ͣ�����һ�ַ�Ӧ���ת������Խ�ߣ�����ҪʹCO��ת���ʴ���ˮ��������0��$\frac{a}{b}$��1��
�ʴ�Ϊ��0��$\frac{a}{b}$��1��
��900��ʱ����CO��H2O��CO2��H2��Ϊ1molʱ��Ũ����Qc=$\frac{0.5��0.5}{0.5��0.5}$=1��0.17=K�����Դ�ʱƽ��Ҫ�����ƶ�����V����V����
�ʴ�Ϊ������
��3����2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g����H1=-1275.6kJ/mol
��2CO ��g��+O2��g��=2CO2��g����H2=-566.0kJ/mol
��H2O��g��=H2O��l����H3=-44.0kJ/mol
��$\frac{��-��+�ۡ�4}{2}$�ã�CH3OH��l��+O2��g��=CO ��g��+2H2O��l����H=$\frac{-1275.6kJ/mol-��-566.0kJ/mol��+��-44.0kJ/mol����4}{2}$=-442.8KJ/mol��
�ʴ�Ϊ��CH3OH��l��+O2��g��=CO��g��+2H2O��l����H=-442.8 kJ/mol��
��4�������£���10mL 0.01mol•L-1 H2C2O4��Һ�еμ�10mL 0.01mol•L-1NaOH��Һʱ��H2C2O4��NaOH��Ӧ����NaHC2O4������NaHC2O4��Һ�����ԣ�����Һ��HC2O4-�ĵ���̶ȴ�����ˮ��̶ȣ�����c��C2O42-����c��H2C2O4������������������ˮ�ĵ����HC2O4-�ĵ��룬��c��H+����c��C2O42-����HC2O4-��ˮ��̶Ƚ�С����c��HC2O4-����c��C2O42-����������Һ�и�����Ũ�ȴ�СΪc��Na+����c��HC2O4-����c��H+����c��C2O42-����c��OH-����
�ʴ�Ϊ��c��Na+����c��HC2O4-����c��H+����c��C2O42-����c��OH-����
��5��ԭ��ظ�������������Ӧ�������ڸ����ŵ磬��������������̼�����ˮ���缫��ӦʽΪ��CH3OCH3+16OH--12e-=2CO32-+11H2O��
�ʴ�Ϊ��CH3OCH3+16OH--12e-=2CO32-+11H2O��
���� ����Ϊ�ۺ��⣬�����Ȼ�ѧ����ʽ����д����ѧƽ��״̬�жϵı�־��ƽ�ⳣ���ļ��㼰��ѧƽ���ƶ�ԭ������˹���ɵļ���Ӧ�á�����Ũ�ȴ�С�ıȽϡ����ط�Ӧԭ�����缫��Ӧʽ����д����ȷ��ѧƽ��������ۣ���Ϥ��˹���ɼ��㷴Ӧ�ȵķ�����ԭ��ع���ԭ���ǽ���ؼ�����Ŀ�Ѷ��еȣ�

 ��һ����ͬ���ɽ�����ϵ�д�
��һ����ͬ���ɽ�����ϵ�д� ������Ӧ���ϵ�д�
������Ӧ���ϵ�д� ��ʦ�㾦�ִʾ��ƪϵ�д�
��ʦ�㾦�ִʾ��ƪϵ�д�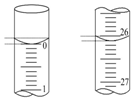 ijѧ����0.100 0mol/L��NaOH����Һ�ζ�δ֪Ũ�ȵ����ᣬ������ɷ�Ϊ���¼�����
ijѧ����0.100 0mol/L��NaOH����Һ�ζ�δ֪Ũ�ȵ����ᣬ������ɷ�Ϊ���¼�����A����ȡ25.00mL����������Һע��ྻ����ƿ��������2��3�η�̪��
B���ñ���Һ��ϴ�ζ���2��3�Σ�
C����ʢ�б���Һ�ļ�ʽ�ζ��̶ܹ��ã����ڵζ��ܼ���ʹ֮������Һ��
D��ȡ��NaOH��Һע���ʽ�ζ������̶���0����2cm��3cm��
E������Һ������0����0�����¿̶Ȳ����¶�����
F������ƿ���ڵζ��ܵ����棬�ñ�NaOH��Һ�ζ����յ㲢�ǵζ���Һ��Ŀ̶ȣ�
�ݴ�ʵ�������գ�
��1����ȷ���������˳����B��D��C��E��A��F���������ĸ��д����
��2������B���������Ŀ���Ƿ�ֹ�ζ����ڱڸ��ŵ�ˮ������Һϡ�Ͷ�������
��3������A�������֮ǰ�����ô�����Һ��ϴ��ƿ����Եζ������Ӱ����ƫ�ߣ�
| �ζ� ���� | ������Һ/mL | 0.100 0mol•L-1NaOH�������mL�� | ||
| �ζ�ǰ | �ζ� | ��Һ���/mL | ||
| ��һ�� | 25.00 | 0.00 | 26.11 | 26.11 |
| �ڶ��� | 25.00 | 1.56 | 30.30 | 28.74 |
| ������ | 25.00 | 0.22 | 26.31 | 26.09 |
��5�����ζ���ʼ�ͽ���ʱ����ʽ�ζ����е�Һ����ͼ��ʾ������ʼ����Ϊ0.00mL���յ����Ϊ26.10mL��
��6��ijѧ����������ʵ��ֱ��¼�й��������ϣ���ѡ�����к�����������ʽ�����������Һ�����ʵ���Ũ�ȣ�c��HCl��=0.1044mol/L��
��Fe2O3��Al2O3�������� ��H2O��I2�����ƾ� ��Na2CO3��NaHCO3����ʯ��ˮ �ܶ��ͣ�ˮ���������Լ�

| A�� | �٢� | B�� | �ڢ� | C�� | �ۢ� | D�� | �ܢ� |
| A�� | ���뼸������ͭ��Һ | B�� | ����������ˮ | ||
| C�� | ��������NaCl��Һ | D�� | �ټ�������ϡ���� |
| A�� | ��ԭ�ӵ�ԭ�ӽṹʾ��ͼ��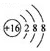 | |
| B�� | ԭ�Ӻ�����10�����ӵ���ԭ��${\;}_{8}^{18}$O | |
| C�� | NH4Cl�ĵ���ʽ��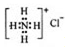 | |
| D�� | ���ȼױ��Ľṹ��ʽ�� |
| A�� | ʵ��������ʯ��ʱ��������ƿ�м���һЩ���Ƭ��Ϊ��ֹ���У��������¿ڽ���ˮ�Ͽڳ���ˮ | |
| B�� | ʵ�����Ʊ�������ʱ���������뱽��Ϻ��ٵμ�Ũ���� | |
| C�� | ʵ��ʹ��ָ��С��մ�ϱ��ӣ�������70�����ϵ���ˮ��ϴ | |
| D�� | ���������Ƿ�ˮ�⣺������Һ��ϡ���������ˮԡ����һ��ʱ�������������Һ��ϼ��ȣ��۲����� |


 ��
�� ��
�� �ж���ͬ���칹�壬���к���1��ȩ����2���ǻ��ķ����廯���ﹲ��
�ж���ͬ���칹�壬���к���1��ȩ����2���ǻ��ķ����廯���ﹲ�� ������ķ�����
������ķ�����
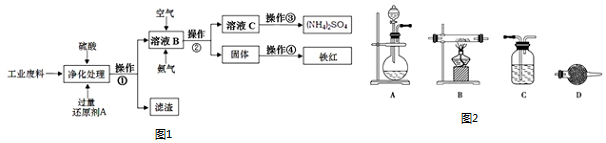
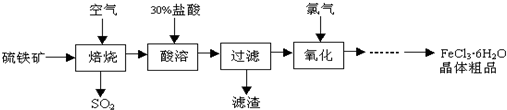
 +6SO2����
+6SO2���� �еĻ�ѧʽΪFe3O4����Ӧ�л��ϼ����ߵ�Ԫ����������
�еĻ�ѧʽΪFe3O4����Ӧ�л��ϼ����ߵ�Ԫ����������