题目内容
8.除去下列物质中的杂质(括号中的物质为杂质),请填写下列空白(注:加入的试剂请填写化学式):
| 物质 | 加入试剂 | 离子方程式 |
| NH4Cl(AlCl3)溶液 | ||
| NaHCO3(Na2CO3)溶液 | ||
| Fe 粉(Al粉) | ||
| FeCl3(FeCl2)溶液 |
 15.(18分)
15.(18分)Ⅰ.下列物质中,不可以通过乙烯加成反应得到的是B(填序号).
A.CH3CH3B.CH3CHCl2
C.CH3CH2OHD.CH3CH2Br
Ⅱ.已知 2CH3CHO+O2 $→_{△}^{催化剂}$ 2CH3COOH.若以乙烯为主要原料合成乙酸,其合成路线如下图所示.
反应②的化学方程式为2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
工业上以乙烯为原料可以生产一种重要的合成有机高分子化合物,其反应的化学方程式为
 ,反应类型是加聚反应.
,反应类型是加聚反应.Ⅲ.某同学欲用乙醇和浓硫酸共热得乙烯,探究过程中发现因温度过高,乙烯气体中可能含有少量的二氧化硫,于是设计下列实验对产物进行验证.
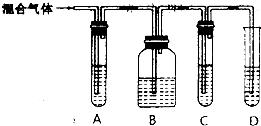
(1)A、B、C、D装置可盛放的试剂是:(将下列需要的试剂序号填入空格内).
A④;B①;C④;D②;
①NaOH溶液 ②溴的四氯化碳溶液 ③浓硫酸 ④品红溶液
(2)确定含有乙烯的现象为溴水褪色,反应的化学方程式:CH2=CH2+Br2→CH2Br-CH2Br
分析 氯化铝与氨水反应生成沉淀和氯化铵;
碳酸钠与二氧化碳、水反应生成碳酸氢钠;
Al与NaOH溶液反应,而Fe不能;
氯化亚铁与氯气反应生成氯化铁;
I.乙烯可与水、HBr、氢气发生加成反应;
II.乙烯为主要原料合成乙酸,由转化可知,A为CH3CH2OH,B为CH3CHO;乙烯发生加聚反应生成高分子化合物;
Ⅲ.(1)二氧化硫是否存在可用品红溶液检验,检验乙烯可以用溴水或高锰酸钾酸性溶液;乙烯和二氧化硫都能使溴水或高锰酸钾酸性溶液褪色;但乙烯不与NaOH溶液反应,二氧化硫能与碱反应(SO2+2NaOH=Na2SO3+H2O),故乙烯的检验应放在排除SO2的干扰后进行,先通过品红溶液褪色检验SO2的存在;再通过NaOH溶液除去SO2,再通过品红溶液不褪色确认SO2已除干净,最后用溴水褪色实验检验乙烯;
(2)根据(1)的分析,最后用溴水褪色实验检验乙烯,乙烯分子含有不饱和碳碳双键,能和溴单质发生加成反应.
解答 解:氯化铝与氨水反应生成氢氧化铝沉淀和氯化铵,则除杂试剂为NH3•H2O,发生的离子反应为Al3++3 NH3•H2O=Al(OH)3↓+3 NH4+;
碳酸钠与二氧化碳、水反应生成碳酸氢钠,则除杂试剂为CO2,发生的离子反应为CO32-+CO2+H2O=2HCO3-;
Al与NaOH溶液反应,而Fe不能,则除杂试剂为NaOH,发生的离子反应为2Al+2OH-+2H2O=2AlO2-+3H2↑;
氯化亚铁与氯气反应生成氯化铁,则除杂试剂为Cl2,发生的离子反应为2Fe2++Cl2=2Fe3++2Cl-,
故答案为:
| 物质 | 加入试剂 | 离子方程式 |
| NH4Cl(AlCl3)溶液 | NH3•H2O | Al3++3 NH3•H2O=Al(OH)3↓+3 NH4+ |
| NaHCO3(Na2CO3)溶液 | CO2 | CO32-+CO2+H2O=2HCO3- |
| Fe 粉(Al粉) | NaOH | 2Al+2OH-+2H2O=2AlO2-+3H2↑ |
| FeCl3(FeCl2)溶液 | Cl2 | 2Fe2++Cl2=2Fe3++2Cl- |
Ⅱ.乙烯与水反应生成乙醇,乙醇催化氧化生成乙醛,乙醛再催化氧化生成乙酸,故反应②为乙醇催化氧化生成乙醛,方程式为:2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O,乙烯结构中含有碳碳双键,能发生加聚反应生成高分子化合物:
 ,反应类型为加聚反应.
,反应类型为加聚反应.故答案为:2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O;
 ;加聚反应;
;加聚反应;Ⅲ.(1)乙烯不与NaOH溶液反应,但二氧化硫能与碱反应(SO2+2NaOH=Na2SO3+H2O),二氧化硫是否存在可用品红溶液检验.乙烯的检验应放在排除SO2的干扰后进行,选通过品红溶液褪色检验SO2的存在;再通过NaOH溶液除去SO2,再通过品红溶液不褪色确认SO2已除干净.最后用溴水褪色实验检验乙烯,
故答案为:④;①;④;②;
(2)根据以上分析,装置D中是用溴水来检验乙烯,溴水溶液褪色,说明含有乙烯,反应的方程式是CH2=CH2+Br2→CH2Br-CH2Br,
故答案为:溴水褪色;CH2=CH2+Br2→CH2Br-CH2Br.
点评 本题考查物质的分离、提纯、有机物合成、性质实验设计等,为高考常见题型和高频考点,侧重于学生的分析能力和实验能力的考查,注意元素化合物及有机物性质综合应用,题目难度不大.

 春雨教育同步作文系列答案
春雨教育同步作文系列答案| A. | 发生的化学反应是复分解反应 | |
| B. | 反应的生成物中有Na2CO3 | |
| C. | 反应后形成的混合物的聚集颗粒直径为1~100nm | |
| D. | 反应说明硅酸易溶于水 |
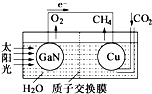 人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.科学家用氮化镓材料与铜组装如图的人工光合系统,成功地实现了以CO2和H2O合成CH4,下列说法不正确的是( )
人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.科学家用氮化镓材料与铜组装如图的人工光合系统,成功地实现了以CO2和H2O合成CH4,下列说法不正确的是( )| A. | 该过程是将太阳能转化为化学能的过程 | |
| B. | GaN表面发生氧化反应,有O2产生 | |
| C. | 电解液中的H+从质子交换膜右侧向左侧迁移 | |
| D. | Cu表面的电极反应式 CO2+8e-+8H+═CH4+2H2O |
| A. | 水泥 | B. | 不锈钢 | C. | 普 通玻璃 | D. | 液氯 |
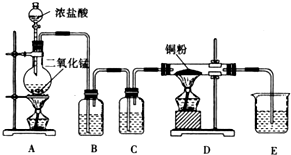 某实验学习小组用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2,装置如图所示.
某实验学习小组用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2,装置如图所示.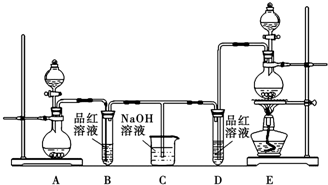
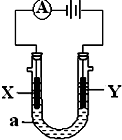 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: