题目内容
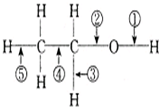 乙醇在一定条件下发生化学反应时化学键断裂如下图所示.下列说法不正确的是( )
乙醇在一定条件下发生化学反应时化学键断裂如下图所示.下列说法不正确的是( )| 反应 | 反应类型 | 断键位置 | |
| A | 乙醇与金属钠 | 置换 | ① |
| B | 乙醇/浓硫酸170℃ | 消去 | ②⑤ |
| C | 乙醇/浓氢溴酸加热 | 取代 | ① |
| 乙醇与乙酸/浓硫酸加热 | 酯化 | ① | |
| D | 乙醇/Cu Ag加热 | 催化氧化 | ①③ |
| 燃烧 | 氧化 | ①②③④⑤ |
| A、A | B、B | C、C | D、D |
考点:乙醇的化学性质
专题:有机物的化学性质及推断
分析:根据乙醇的性质,结合反应物与产物的结构判断.有机反应重在掌握反应的机理即清楚断键与成键位置.
解答:
解:A.乙醇与与金属钠发生置换反应,生成乙醇钠和氢气:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,故乙醇断键的位置为①,故A正确;
B.乙醇和浓H2SO4共热至170℃时,发生消去反应,生成乙烯,反应方程式为CH3CH2OH
CH2═CH2+H2O,故乙醇断键的位置为:②和⑤,故B正确;
C.乙醇与浓溴水共热时,发生取代反应,生成溴乙烷,CH3CH2OH+HBr(浓)→CH3CH2Br+H2O,故乙醇断键的位置为:②;乙醇和CH3COOH共热时,发生酯化反应,生成乙酸乙酯,可以18O标记,研究反应机理,CH3COOH+CH3CH218OH
CH3CO18OCH2CH3+H2O,故乙醇断键的位置为:①,故C错误;
D.乙醇在Ag催化下与O2反应生成乙醛和水:2CH3CH2OH+O2
2CH3CHO+2H2O,故乙醇断键的位置为①和③;燃烧是有机物最剧烈的反应,生成二氧化碳和水,所有的化学键都要断裂,故乙醇断键的位置为①②③④⑤,故D正确;
故选C.
B.乙醇和浓H2SO4共热至170℃时,发生消去反应,生成乙烯,反应方程式为CH3CH2OH
| ||
| 170℃ |
C.乙醇与浓溴水共热时,发生取代反应,生成溴乙烷,CH3CH2OH+HBr(浓)→CH3CH2Br+H2O,故乙醇断键的位置为:②;乙醇和CH3COOH共热时,发生酯化反应,生成乙酸乙酯,可以18O标记,研究反应机理,CH3COOH+CH3CH218OH
| ||
| △ |
D.乙醇在Ag催化下与O2反应生成乙醛和水:2CH3CH2OH+O2
| ||
| △ |
故选C.
点评:本题考查乙醇的性质,难度不大,了解反应的机理是解题的关键.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
甲酸、乙酸、碳酸、苯酚的酸性由强到弱的顺序是( )
| A、碳酸、苯酚、甲酸、乙酸 |
| B、甲酸、乙酸、碳酸、苯酚 |
| C、甲酸、碳酸、苯酚、乙酸 |
| D、苯酚、碳酸、乙酸、甲酸 |
下列事实、事件、事故中与甲烷有无关的是( )
| A、天然气的主要成分 |
| B、石油经过催化裂化及裂解后的主要产物 |
| C、“西气东输”中气体 |
| D、煤矿中的瓦斯爆炸 |
化学反应经常伴随着颜色变化,下列关于颜色的叙述正确的是( )
①钾的焰色反应--紫色
②淀粉碘化钾溶液遇碘离子--蓝色
③溴化银见光分解--白色
④适量的氯气通入KBr溶液--橙黄色
⑤新制氯水久置后--无色
⑥铜在氯气中燃烧产生的烟--棕黄色.
①钾的焰色反应--紫色
②淀粉碘化钾溶液遇碘离子--蓝色
③溴化银见光分解--白色
④适量的氯气通入KBr溶液--橙黄色
⑤新制氯水久置后--无色
⑥铜在氯气中燃烧产生的烟--棕黄色.
| A、①②③⑤ | B、①④⑤⑥ |
| C、②③④⑥ | D、①③⑤⑥ |
下列物质不能使酸性KMnO4溶液退色的是( )
| A、C4H10 |
| B、C2H2 |
C、 |
| D、CH3COOH |
下列物质不能使溴水褪色的是( )
| A、乙烯 |
| B、二氧化硫 |
| C、KI溶液 |
| D、CH4 |
下列说法错误的是( )
| A、2H2S+SO2=3S+2H2O中,氧化产物和还原产物物质的量之比为2:1 | ||||
| B、4Zn+10HNO3=4Zn(NO3)2+NH4NO3+3H2O中,氧化剂和还原剂物质的量之比为5:2 | ||||
C、3I2+6KOH
| ||||
D、2FeS+6H2SO4(浓)
|
一定温度下,10mL 0.40mol/L H2O2溶液发生催化分解.不同时刻测得生成O2的体积(已折算为标准状况)如下表.
下列叙述不正确的是(溶液体积变化忽略不计)( )
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
| A、0~6min的平均反应速率:v(H2O2)≈3.3×10-2mol/(L?min) |
| B、6~10min的平均反应速率:v(H202)<3.3×10-2mol/(L?min) |
| C、反应至6min时,c(H2O2)=0.30mol/L |
| D、反应至6min时,H2O2分解了50% |
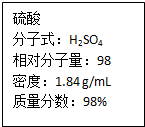 如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题: