题目内容
13.海水的综合利用包括很多方面,下图是从海水中通过一系列工艺流程提取产品的流程图.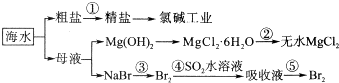
海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-等离子.
已知:MgCl2•6H2O受热生成Mg(OH)Cl和HCl气体等.回答下列问题:
(1)海水pH约为8的原因主要是天然海水含上述离子中的HCO3-.
(2)除去粗盐溶液中的杂质(Mg2+、SO42-、Ca2+),加入药品的顺序可以为①②④③.
①NaOH溶液 ②BaCl2溶液 ③过滤后加盐酸 ④Na2CO3溶液
(3)过程②中由MgCl2•6H2O制得无水MgCl2,应如何操作在HCl气流中脱水,抑制氯化镁水解,加热至恒重.
(4)从能量角度来看,氯碱工业中的电解饱和食盐水是一个将电能转化为化学能的过程.采用石墨阳极,不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式Mg+2H2O=Mg(OH)2↓+H2↑.
(5)从第③步到第④步的目的是浓缩富集溴.采用“空气吹出法”从浓海水中吹出Br2,并用SO2吸收.主要反应的化学方程式为Br2+SO2+2H2O=H2SO4+2HBr.
分析 海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-等离子,可分别加热氯化钡、氢氧化钠、碳酸钠,过滤后加入盐酸,结晶得到精盐,可用于氯碱工业;母液中含有镁离子,加入氢氧化钠得到氢氧化镁,加入盐酸得到氯化镁晶体,在盐酸氛围中加热得到无水氯化镁;溴化钠中通入氯气得到溴,用二氧化硫吸收得到亚硫酸钠,继续通入氯气,得到溴,
(1)海水中的弱酸根离子水解显碱性;
(2)根据镁离子用氢氧根离子沉淀,硫酸根离子用钡离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀,最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子,进行分析解答;
(3)氯化镁易水解,为防止水解过程③中结晶出的MgCl2•6H2O要一定条件下加热脱水制得无水MgCl2;
(4)电解饱和食盐水是电能转化为化学能,惰性电极电极熔融氯化镁生成氯气和金属镁,镁和水反应生成氢氧化镁和氢气;
(5)溴离子被氧化为溴单质后,被二氧化硫吸收生成溴离子,加入氧化剂氧化溴离子为溴单质,富集溴元素;采用“空气吹出法”从浓海水中吹出Br2,并用SO2吸收利用二氧化硫还原性和溴单质反应生成硫酸和HBr.
解答 解:海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-等离子,可分别加热氯化钡、氢氧化钠、碳酸钠,过滤后加入盐酸,结晶得到精盐,可用于氯碱工业;母液中含有镁离子,加入氢氧化钠得到氢氧化镁,加入盐酸得到氯化镁晶体,在盐酸氛围中加热得到无水氯化镁;溴化钠中通入氯气得到溴,用二氧化硫吸收得到亚硫酸钠,继续通入氯气,得到溴,
(1)海水中主要含有Na+、K+、Mg2+、Cl-、SO42-、Br-、HCO3-等离子,在这些离子中能发生水解的是CO32-、HCO-3离子,HCO3-+H2O?H2CO3+OH-它们水解呈碱性,所以天然海水的pH≈8,呈弱碱性,
故答案为:HCO3-;
(2)镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可溶液以将镁离子沉淀;硫酸根离子用钡离子沉淀,加入过量的氯化钡溶液可以将硫酸根离子沉淀;至于先除镁离子,还是先除硫酸根离子都可以;钙离子用碳酸根离子沉淀,除钙离子加入过量的碳酸钠溶液转化为沉淀,但是加入碳酸钠溶液要放在加入的氯化钡溶液之后,这样碳酸钠会除去反应剩余的氯化钡;完全反应后,再进行过滤,最后再加入适量盐酸除去反应剩余的氢氧根离子和碳酸根离子,故正确的顺序为:①②④⑤,
故答案为:①②④③;
(3)镁离子水解,应抑制其水解得到无水盐,所以利用MgCl2•6H2O制得无水氯化镁,应采取的措施是在HCl气流中脱水,抑制氯化镁水解,
故答案为:在HCl气流中脱水,抑制氯化镁水解,加热至恒重;
(4)电解原理分析,电解饱和食盐水是电能转化为化学能,采用石墨阳极,不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑,电解时,若有少量水存在会造成产品镁的消耗,发生反应为镁和水反应生成氢氧化镁和氢气,反应的化学方程式为:Mg+2H2O=Mg(OH)2↓+H2↑,
故答案为:电能;化学能;MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;Mg+2H2O=Mg(OH)2↓+H2↑;
(5)溴离子被氧化为溴单质后,被二氧化硫吸收生成溴离子,加入氧化剂氧化溴离子为溴单质,富集溴元素,从第③步到第⑤步的目的是为了浓缩富集溴,采用“空气吹出法”从浓海水中吹出Br2,并用SO2吸收,溴单质和二氧化硫发生氧化还原反应生成硫酸和氢溴酸,发生反应的化学方程式为:Br2+SO2+2H2O=H2SO4+2HBr,
故答案为:浓缩富集溴;Br2+SO2+2H2O=H2SO4+2HBr.
点评 本题考查物质的分离、提纯,为高考常见题型,侧重于学生的分析能力、实验能力的考查,题目涉及海水资源综合利用、离子的除杂、氧化还原反应、元素及其化合物的有关知识进行综合利用,提高了试题的综合性,难度中等.

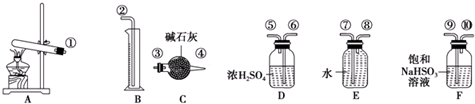
【提出猜想】
Ⅰ.所得气体的成分可能只含SO3一种;
Ⅱ.所得气体的成分可能含有SO2、O2两种;
Ⅲ.所得气体的成分可能含有SO3、SO2、O2三种.
【实验探究】
实验操作过程略.
已知实验结束时,硫酸铜完全分解.
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口的连接顺序为:①→⑨→⑩→⑥→⑤→③→④→⑧→⑦→②(填接口序号).
(2)若实验结束时B中量筒没有收集到水,则证明猜想Ⅰ正确.
(3)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同,数据如下:
| 实验小组 | 称取CuSO4的质量/g | 装置C增加的质量/g | 量筒中水的体积折算成标准状况下气体的体积/mL |
| 一 | 6.4 | 2.56 | 448 |
| 二 | 6.4 | 2.56 | 224 |
第一小组:2CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+2SO2↑+O2↑;
第二小组:4CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$4CuO+2SO2↑+2SO3↑+O2↑.
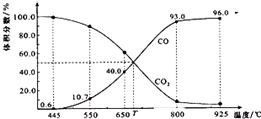 一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如图所示:已知:气体分压(p分)=气体总压(p总)×体积分数.下列说法正确的是( )
一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如图所示:已知:气体分压(p分)=气体总压(p总)×体积分数.下列说法正确的是( )| A. | 550℃时,若充入惰性气体,v正、v逆 均减小,平衡不移动 | |
| B. | 650℃时,反应达平衡后CO2的转化率为25.0% | |
| C. | T℃时,若充入等体积的CO2和CO,平衡不移动 | |
| D. | 925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=24.p总 |
 氮及其化合物在工业生产和国防建设中有广泛应用.回答下列问题:
氮及其化合物在工业生产和国防建设中有广泛应用.回答下列问题:(1)氮气性质稳定,可用作保护气.请用电子式表示氮气的形成过程:
 .
.(2)联氨(N2H4)是一种还原剂.已知:H2O(l)═H2O(g)△H=+44kJ/mol.试结合下表数据,写出N2H4 (g)燃烧热的热化学方程式:N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=-631.7kJ/mol.
| 化学键 | N-H | N-N | N═N | N≡N | O═O | O-H |
| 键能(kJ/mol) | 390.8 | 193 | 418 | 946 | 497.3 | 462.8 |
(4)氨的催化氧化用于工业生产硝酸.该反应可设计成新型电池,试写出碱性环境下,该电池的负极电极反应式:NH3-5e-+5OH-=NO+4H2O.
(5)将某浓度的NO2气体充入一恒容绝热容器中,发生反应2NO2?N2O4其相关图象如图.
①0~3s时v(NO2)增大的原因是容器为绝热体系,该反应正向进行放热,体系温度升高,v(NO2)增大.
②5s时NO2转化率为75%.
| A. | 58.5 g的氯化钠固体中含有NA个氯化钠分子 | |
| B. | 标准状况下,5.6 L一氧化氮和5.6 L氧气混合后的分子总数为0.5NA | |
| C. | 0.1 mol•L-1氢氧化钠溶液中含钠离子数为0.1NA | |
| D. | 5.6 g铁与足量稀硫酸反应时失去电子数为0.2NA |
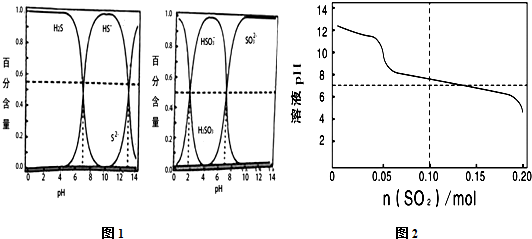
| A. | 由图1的一级电离与二级电离的Ka值可知H2SO3?2H++SO32- Ka≈10-7 | |
| B. | 向1L0.1 mol•L-1的Na2S溶液中持续通入SO2气体达到0.1 mol时,溶液中H2S、HS-、HSO3-、SO32-可同时一定量共存 | |
| C. | 向1L0.1 mol•L-1的Na2S溶液中持续通入SO2气体达到0.1 mol时,溶液中存在如下关系:c(H+)+c(Na+)═c(OH-)+2c(S2-)+2c(SO32-)+c(HS- )+c(HSO3-) | |
| D. | 在反应过程中当pH降至7.5左右,之后可能出现淡黄色沉淀 |
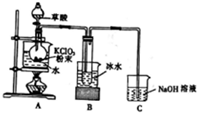 二氧化氯(ClO2)是一种高效消毒剂,在60℃时用氯酸钾与草酸(中强酸)反应可制备二氧化氯,实验装置如图所示.已知:通常情况下,二氧化氯的沸点为11.0℃,极易爆炸,制取和使用二氧化氯时要用性质确定的气体稀释,以防爆炸,回答下列问题:
二氧化氯(ClO2)是一种高效消毒剂,在60℃时用氯酸钾与草酸(中强酸)反应可制备二氧化氯,实验装置如图所示.已知:通常情况下,二氧化氯的沸点为11.0℃,极易爆炸,制取和使用二氧化氯时要用性质确定的气体稀释,以防爆炸,回答下列问题: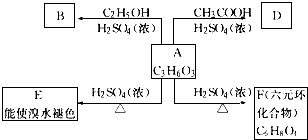
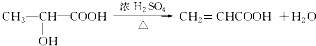 ;A→F
;A→F