题目内容
向一种溶液中滴加另一种溶液后,溶液的颜色不发生变化的是( )
| A、碳酸钠溶液中滴加稀硫酸 |
| B、氯化铁溶液中滴加硫氰化钾溶液 |
| C、碘水中滴加淀粉碘化钾溶液 |
| D、酸性高锰酸钾溶液中滴加亚硫酸钠溶液 |
考点:钠的重要化合物,二价Fe离子和三价Fe离子的检验,食物中淀粉、蛋白质、葡萄糖的检验
专题:几种重要的金属及其化合物
分析:A.溶液无色,生成无色气体;
B.生成Fe(SCN)3,溶液呈血红色;
C.淀粉遇碘变蓝色;
D.高锰酸钾与亚硫酸钠发生氧化还原反应.
B.生成Fe(SCN)3,溶液呈血红色;
C.淀粉遇碘变蓝色;
D.高锰酸钾与亚硫酸钠发生氧化还原反应.
解答:
解:A.溶液无色,生成无色气体,没有颜色变化,故A正确;
B.氯化铁溶液呈黄色,加入KSCN,生成Fe(SCN)3,溶液呈血红色,有颜色变化,故B错误;
C.淀粉遇碘变蓝色,故C错误;
D.高锰酸钾与亚硫酸钠发生氧化还原反应,溶液变为无色,故D错误.
故选A.
B.氯化铁溶液呈黄色,加入KSCN,生成Fe(SCN)3,溶液呈血红色,有颜色变化,故B错误;
C.淀粉遇碘变蓝色,故C错误;
D.高锰酸钾与亚硫酸钠发生氧化还原反应,溶液变为无色,故D错误.
故选A.
点评:本题考查较为综合,涉及物质的颜色的变化,为高频考点,侧重于元素化合物知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
对于有机物 ,下列说法中正确的是( )
,下列说法中正确的是( )
 ,下列说法中正确的是( )
,下列说法中正确的是( )| A、它是苯酚的同系物 |
| B、1 mol该有机物能与溴水反应消耗2 mol Br2发生取代反应 |
| C、1 mol该有机物能与金属钠反应生成0.5 mol H2 |
| D、1 mol该有机物能与2 mol NaOH反应 |
把①蔗糖 ②麦芽糖 ③淀粉 ④纤维素 ⑤油脂 ⑥酶 ⑦蛋白质,在酸存在的条件下分别进行水解,其水解的最终产物只有1种的有( )
| A、①②③④⑤ | B、②③④ |
| C、④⑥⑦ | D、③④⑤⑥⑦ |
下列反应中,浓硫酸只表现出酸性的是( )
| A、与氢氧化钠反应 |
| B、与铜共热 |
| C、与氧化铜反应 |
| D、与木炭共热 |
已知:
①1mol H2分子中化学键断裂时需要吸收436kJ的能量,
②1mol I2蒸气中化学键断裂时需要吸收151kJ的能量,
③由H原子和I原子形成1mol HI分子时释放299kJ的能量.
下列热化学方程式正确的是( )
①1mol H2分子中化学键断裂时需要吸收436kJ的能量,
②1mol I2蒸气中化学键断裂时需要吸收151kJ的能量,
③由H原子和I原子形成1mol HI分子时释放299kJ的能量.
下列热化学方程式正确的是( )
| A、2HI(g)=H2(g)+I2(g);△H=+11 kJ?mol-1 |
| B、H2(g)+I2(g)=HI(g);△H=-11 kJ?mol-1 |
| C、H2(g)+I2(g)=2HI(g);△H=+288 kJ?mol-1 |
| D、H2(g)+I2(g)=HI(g);△H=-114 kJ?mol-1 |
 丹参素能明显抑制血小板的聚集,其结构如图所示,下列说法错误的是( )
丹参素能明显抑制血小板的聚集,其结构如图所示,下列说法错误的是( )| A、丹参素的分子式为C9H10O5 |
| B、丹参素能发生缩聚、消去、氧化反应 |
| C、1 mol丹参素最多可以和3mol H2发生加成反应 |
| D、1 mol丹参素与足量Na2CO3发生反应最多可生成二氧化碳1.5mol |
 在实验室进行工业合成氨的模拟实验:
在实验室进行工业合成氨的模拟实验: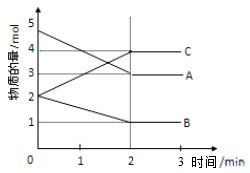 某温度时,在一恒容密闭容器中,A、B、C三种物质的物质的量n(mol)随时间t(min)变化的曲线如图所示,从图中的数据分析:
某温度时,在一恒容密闭容器中,A、B、C三种物质的物质的量n(mol)随时间t(min)变化的曲线如图所示,从图中的数据分析: