题目内容
下列物质能用来干燥CO2气体的是( )
| A、浓H2SO4 |
| B、碱石灰 |
| C、氧化钙 |
| D、氢氧化钠 |
考点:气体的净化和干燥
专题:化学实验基本操作
分析:二氧化碳为酸性气体,可以用酸性或者中性干燥剂干燥,但不能使用碱性干燥剂干燥,如碱石灰、氢氧化钠、氧化钙等为碱性干燥剂,不能用于干燥二氧化碳,据此进行解答.
解答:
解:A.浓硫酸为酸性干燥剂,能够干燥二氧化碳气体,故A正确;
B.碱石灰为碱性干燥剂,不能干燥酸性气体二氧化碳,故B错误;
C.氧化钙为碱性干燥剂,不能干燥酸性气体二氧化碳,故C错误;
D.氢氧化钠为碱性干燥剂,不能干燥二氧化碳气体,故D错误;
故选A.
B.碱石灰为碱性干燥剂,不能干燥酸性气体二氧化碳,故B错误;
C.氧化钙为碱性干燥剂,不能干燥酸性气体二氧化碳,故C错误;
D.氢氧化钠为碱性干燥剂,不能干燥二氧化碳气体,故D错误;
故选A.
点评:本题考查了气体的净化与干燥,题目难度不大,注意掌握常见气体的性质及干燥剂的类型、选用方法,明确浓硫酸为酸性、强氧化性的干燥剂,不能干燥具有还原性、碱性的气体.

练习册系列答案
相关题目
金属晶体的下列性质中,不能用金属晶体结构加以解释的是( )
| A、易导电 | B、易导热 |
| C、有延展性 | D、易锈蚀 |
下列叙述正确的是( )
| A、Li在氧气中燃烧主要生成Li2O2 | ||||
| B、实验室制备Cl2可用排饱和食盐水集气法收集 | ||||
C、
| ||||
| D、碱金属和卤素的单质的熔沸点随原子序数递增均依次升高 |
卤素单质与氢气都能反应,反应产物是卤化氢(X2+H2=2HX),这是卤素性质的相似性;但其反应条件不同,从“黑暗中即可剧烈爆炸”→“不断加热才能缓慢反应”,这是其性质的递变性,其性质递变性原因是( )
| A、最外层电子数相同 |
| B、都是双原子分子 |
| C、电子层数不同 |
| D、卤化氢中卤素都是-1价 |
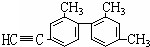 已知碳碳单键可以绕键轴自由旋转,结构简式为如图所示的烃,下列说法中正确的是( )
已知碳碳单键可以绕键轴自由旋转,结构简式为如图所示的烃,下列说法中正确的是( )| A、分子中处于同一直线上的碳原子最多有7个 |
| B、分子中至少有12个碳原子处于同一平面上 |
| C、该烃苯环上的一氯代物共有3种 |
| D、该烃苯环上一氯代物共有5种 |
在55℃时,下列说法正确的是( )
| A、向水中加入少量硫酸氢钠固体,促进了水的电离,c(H+)增大,Kw不变 |
| B、pH=3的盐酸和pH=11的氨水等体积混合,溶液显碱性 |
| C、0.1mol/L的(NH4)2SO4溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| D、pH=8的NaHCO3溶液中:c(OH-)=1×10-6mol/L |
下列叙述中正确的是( )
| A、“A氧化B”与“B被A氧化”,“A被B还原”表达的含义相同 |
| B、失电子越多的还原剂,其还原性就越强 |
| C、阳离子只能得电子被还原,作氧化剂 |
| D、含有最高价元素的化合物一定具有强氧化性 |
针铁矿(式量为89)组成元素是Fe、O和H,下列判断错误的是( )
| A、完全溶解89g针铁矿,需要1.0mol/L的稀盐酸至少2L |
| B、针铁矿的化学式是FeO(OH) |
| C、针铁矿中铁元素为+3价 |
| D、44.5g针铁矿约含有6.02×1023个O原子 |
下列各组离子在指定的溶液中一定能大量共存的是( )
| A、含有大量Fe3+的溶液:Na+、SCN-、Cl-、I- |
| B、氯水溶液:H+、Fe2+、Cl-、SO42- |
| C、常温下,pH=12的溶液:K+、Cl-、SO42-、SiO2- |
| D、与铝粉反应放出氢气的无色溶液中:Na+、NH4+、SO42-、AlO2- |