题目内容
铁单质及其化合物在生活、生产中应用广泛.请回答下列问题:
(1)硫酸铁可做絮凝剂,常用于净水,其原理是 (用离子方程式表示)
(2)磁铁矿冶炼铁的原理是Fe3O4+4CO
3Fe+4CO2,若有1.5mol Fe3O4参加反应,转移的电子的物质的量是 .
(3)由于氧化性Fe3+>Cu2+,氯化铁溶液常用做印刷电路铜板腐蚀剂,反应的离子方程式是 .
(1)硫酸铁可做絮凝剂,常用于净水,其原理是
(2)磁铁矿冶炼铁的原理是Fe3O4+4CO
| ||
(3)由于氧化性Fe3+>Cu2+,氯化铁溶液常用做印刷电路铜板腐蚀剂,反应的离子方程式是
考点:铁的氧化物和氢氧化物,氧化还原反应的电子转移数目计算,铁盐和亚铁盐的相互转变
专题:元素及其化合物
分析:(1)三价铁水解生成的氢氧化铁胶体具有净水作用;
(2)氧化还原反应中,化合价升高值=化合价降低值=转移电子数;
(3)金属铜可以和三价铁之间发生氧化还原反应.
(2)氧化还原反应中,化合价升高值=化合价降低值=转移电子数;
(3)金属铜可以和三价铁之间发生氧化还原反应.
解答:
解:(1)三价铁水解生成的氢氧化铁胶体具有净水作用,原理方程式为:Fe3++3H2O?Fe(OH)3+3H+,
故答案为:Fe3++3H2O?Fe(OH)3+3H+;
(2)氧化还原反应Fe3O4+4CO
3Fe+4CO2中,化合价升高值=化合价降低值=转移电子数=8,即有1mol Fe3O4参加反应,转移电子的物质的量是8mol,所以有1.5mol Fe3O4参加反应,转移电子的物质的量是12mol,
故答案为:12mol;
(3)三价铁的氧化性强于铜离子,所以金属铜可以和三价铁之间发生氧化还原反应:Cu+2Fe3+=2Fe2++Cu2+,
故答案为:Cu+2Fe3+=2Fe2++Cu2+.
故答案为:Fe3++3H2O?Fe(OH)3+3H+;
(2)氧化还原反应Fe3O4+4CO
| ||
故答案为:12mol;
(3)三价铁的氧化性强于铜离子,所以金属铜可以和三价铁之间发生氧化还原反应:Cu+2Fe3+=2Fe2++Cu2+,
故答案为:Cu+2Fe3+=2Fe2++Cu2+.
点评:本题主要考查对化学基本概念和原理的理解,以及利用课本知识解决新问题能力,主要考查氧化还原反应的规律运用和电子转移的计算,盐类水解的应用等知识,难度中等.

练习册系列答案
相关题目
能说明醋酸是弱电解质的依据是( )
| A、醋酸能与碳酸钠反应,并有二氧化碳气体生成 |
| B、醋酸溶液能使紫色石蕊试液变红 |
| C、用醋酸溶液做导电性实验时,灯泡较暗 |
| D、在pH相等的醋酸和盐酸中,前者的物质的量浓度大得多 |
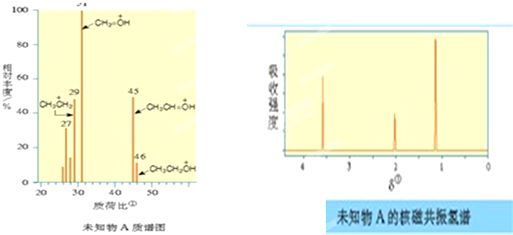


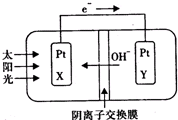 近年来C02的利用日新月异.
近年来C02的利用日新月异.