题目内容
12.NA为阿伏伽德罗常数的值,下列说法正确的是( )| A. | 常温常压下,92g的NO2和N2O4混合气体所含的原子数为6NA | |
| B. | 标准状况下,将22.4LCl2通入足量的NaOH溶液中,转移的电子数为2NA | |
| C. | 1molFeCl3完全转化为Fe(OH)3胶体后生成胶粒个数为NA | |
| D. | 0.1L0.5mol/LCH3COOH溶液中的H+个数为0.05NA |
分析 A、NO2和N2O4的最简式均为NO2;
B、求出氯气的物质的量,然后根据氯气和碱的反应为歧化反应来分析;
C、一个氢氧化铁胶粒是多个氢氧化铁的聚集体;
D、醋酸是弱电解质.
解答 解:A、NO2和N2O4的最简式均为NO2,故92g混合物中含有的NO2的物质的量为2mol,故含6NA个原子,故A正确;
B、标况下22.4L氯气的物质的量为1mol,而氯气和碱的反应为歧化反应,故1mol氯气转移1NA个电子,故B错误;
C、一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故1mol氯化铁形成的氢氧化铁胶粒的个数小于NA个,故C错误;
D、醋酸是弱电解质,故不能完全电离,故溶液中的氢离子的个数小于0.05NA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
相关题目
3.如图所示,下列实验现象预测或操作正确的是( )
| A. | 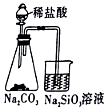 如图,可以证明非金属性强弱:Cl>C>Si | |
| B. | 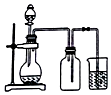 如图,用铜片和稀硝酸制NO | |
| C. | 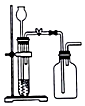 如图,用锌粒和稀硫酸制H2 | |
| D. | 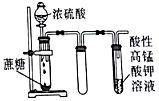 如图,酸性KMnO4溶液中有气泡出现,且溶液颜色会逐渐变浅乃至褪去 |
20.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1mol•L-1的NaClO溶液中含有ClO-的数目小于NA | |
| B. | Na2O2与足量CO2反应生成1molO2,转移的电子数目为2NA | |
| C. | 两份2.7g铝分别与100mL浓度为2mol•L-1的盐酸和氢氧化钠溶液充分反应,转移的电子数均为0.3NA | |
| D. | 18g重水(D2O)所含的电子数为10NA |
7.下列离子组在指定溶液中能大量共存的是( )
| A. | 在含有大量HCO3-的溶液中:K+、Na+、Al3+、Br- | |
| B. | 使pH试纸变蓝的溶液中:NH4+、Na+、Cl-、ClO- | |
| C. | 含有0.1 mol•L-1Br-离子的溶液中:Cl-、Fe3+、Al3+、Cu2+ | |
| D. | 能使甲基橙变红的溶液中:Na+、K+、SO42-、AlO2- |
9.用下列实验装置进行相应实验,能达到实验目的是( )


| A. | 用装置甲制取氨气 | B. | 用装置乙制取少量纯净的CO2气体 | ||
| C. | 用装置丙验证氨气具有还原性 | D. | 用装置丁吸收尾气氨气 |
6.氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
| A. | 分散质颗粒直径都在l~100nm之间 | B. | 都透过半透膜 | ||
| C. | 都是透明的澄清液体 | D. | 都呈红褐色 |
7.下列说法正确的是( )
| A. | 石英玻璃主要成分是硅酸盐 | |
| B. | 太阳能电池可采用二氧化硅材料制作,其应用有利于环保、节能 | |
| C. | 木材浸泡在硅酸钙溶液可以防腐和防火 | |
| D. | 工艺师利用氢氟酸刻蚀石英制作艺术品 |