题目内容
18.下列比较正确的是 ( )①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4
④碱性:Ca(OH)2>Mg(OH)2.
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
分析 ①元素的非金属性越强,对应的氢化物越稳定;
②根据同周期元素从左到右原子半径逐渐减小,同主族元素从上到下原子半径逐渐增大判断;
③元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
④元素的金属性越强,对应的最高价氧化物的水化物的碱性越强.
解答 解:①非金属性F>O>S,元素的非金属性越强,对应的氢化物越稳定,所以稳定性:HF>H2O>H2S,故①错误;
②同周期元素从左到右原子半径逐渐减小,则原子半径Na>Mg,一般来说,原子核外电子层数越多,原子半径越大,则Na>Mg>O,故②正确;
③非金属性Cl>S>P,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,所以酸性:H3PO4<H2SO4<HClO4 故③错误;
④金属性Ca>Mg,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,故④正确;
故选B.
点评 本题考查元素周期律知识,侧重于学生的分析能力和基本概念的理解和运用的考查,注意元素的性质与对应单质、化合物的关系,把握元素周期律的递变规律是解答该类题目的关键,难度不大.

练习册系列答案
相关题目
6.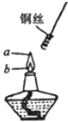 如图,某同学做乙醇氧化实验时,将螺旋状铜丝先放到a点处加热,然后再移到b点,发现铜丝在火焰a、b两点时现象明显不同.请你写出a、b两点的实验现象,并解释产生该现象的原因,并写出化学反应方程式.
如图,某同学做乙醇氧化实验时,将螺旋状铜丝先放到a点处加热,然后再移到b点,发现铜丝在火焰a、b两点时现象明显不同.请你写出a、b两点的实验现象,并解释产生该现象的原因,并写出化学反应方程式.
 如图,某同学做乙醇氧化实验时,将螺旋状铜丝先放到a点处加热,然后再移到b点,发现铜丝在火焰a、b两点时现象明显不同.请你写出a、b两点的实验现象,并解释产生该现象的原因,并写出化学反应方程式.
如图,某同学做乙醇氧化实验时,将螺旋状铜丝先放到a点处加热,然后再移到b点,发现铜丝在火焰a、b两点时现象明显不同.请你写出a、b两点的实验现象,并解释产生该现象的原因,并写出化学反应方程式.| 实验现象 | 解释 | 化学方程式 | |
| a | |||
| b |
13.设NA 表示阿伏加德罗常数,下列说法正确的是( )
| A. | 常温常压下,11.2 L氯气所含有的原子数目为NA | |
| B. | 9 g水所含有的氢原子数目为NA | |
| C. | 在同温同压时,相同物质的量的任何气体的体积相同且为11.2L | |
| D. | 0.1 mol甲烷分子含有的原子数目为NA |
7.下列物质的用途中,不正确的是( )
| A. | Na2O2作呼吸面具中的供氧剂 | |
| B. | 硫磺用于制火药 | |
| C. | 镁合金用于制造汽车、飞机、火箭 | |
| D. | BaCO3作“钡餐”--检查肠胃的内服药 |
8.联合国气候变化大会2009年12月7日在丹麦首都哥本哈根拉开帷幕,很多人称这次大会为“人类拯救地球的最后机会“.据报道,在火星和金星大气层中发现了一种非常特殊的会导致温室效应的气态化合物,它的结构式为:16O=C=18O.下列说法正确的是( )
| A. | 16O与18O为同种核素 | |
| B. | 16O=C=18O与16O=C=16O互为同位素 | |
| C. | 16O=C=18O的化学性质与16O=C=16O几乎完全相同 | |
| D. | 16O=C=18O的摩尔质量为46g |
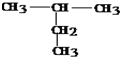 :2-甲基丁烷
:2-甲基丁烷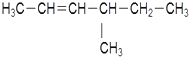 :4-甲基-2-己烯
:4-甲基-2-己烯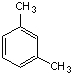 1,3-二甲苯.
1,3-二甲苯.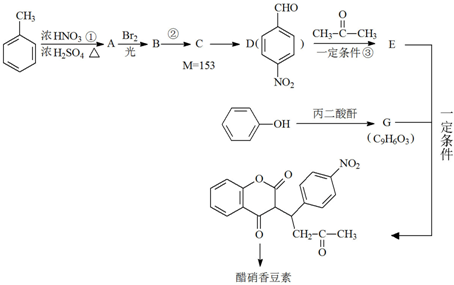
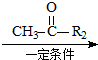 R1-CH=
R1-CH=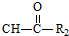 +H2O
+H2O 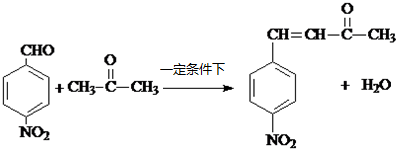
 .
. .
.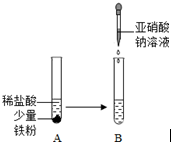 亚硝酸钠(NaNO2)俗称工业盐,外观和食盐相似,有咸味,易溶于水,水溶液显碱性,加强热时能分解产生有刺激性气味的气体,人若误食会引起中毒,致死量为0.3g~0.5g,它使人中毒是因为它能将人体血红蛋白中的Fe2+转化为Fe3+,从而使血红蛋白丧失携氧能力.
亚硝酸钠(NaNO2)俗称工业盐,外观和食盐相似,有咸味,易溶于水,水溶液显碱性,加强热时能分解产生有刺激性气味的气体,人若误食会引起中毒,致死量为0.3g~0.5g,它使人中毒是因为它能将人体血红蛋白中的Fe2+转化为Fe3+,从而使血红蛋白丧失携氧能力.