题目内容
13.设NA 表示阿伏加德罗常数,下列说法正确的是( )| A. | 常温常压下,11.2 L氯气所含有的原子数目为NA | |
| B. | 9 g水所含有的氢原子数目为NA | |
| C. | 在同温同压时,相同物质的量的任何气体的体积相同且为11.2L | |
| D. | 0.1 mol甲烷分子含有的原子数目为NA |
分析 A、常温常压下,气体摩尔体积大于22.4L/mol;
B、求出水的物质的量,然后根据1mol水中含2mol氢原子来分析;
C、同温同压下,气体摩尔体积相同但不一定是22.4L/mol;
D、甲烷是5原子分子.
解答 解:A、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L氯气的物质的量小于0.5mol,则含有的原子的物质的量小于1mol,即小于NA个,故A错误;
B、9g水的物质的量n=$\frac{9g}{18g/mol}$=0.5mol,而1mol水中含2mol氢原子,故0.5mol水中含1mol氢原子,即NA个,故B正确;
C、同温同压下,气体摩尔体积相同,但不一定是22.4L/mol,且相同物质的量的气体的物质的量也不一定是1mol,故只能说同温同压下,相同物质的量的任何气体的体积相同,但体积无法确定,故C错误;
D、甲烷是5原子分子,即1mol甲烷含5mol原子,则0.1mol甲烷含0.5mol原子,即0.5NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
1.下列各组物质中,化学键类型和化合物类型都相同的是( )
| A. | CO2和Na2CO3 | B. | SO2和H2O | C. | KOH和NaCl | D. | NaCl和HCl |
8.今有A、B两种原子,A原子的M层比B原子的M层多1个电子,B原子的L层电子数是A原子L层电子数的一半.A和B分别为( )
| A. | Na和Mg | B. | Na和C | C. | Mg和Al | D. | C和Mg |
18.下列比较正确的是 ( )
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4
④碱性:Ca(OH)2>Mg(OH)2.
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4
④碱性:Ca(OH)2>Mg(OH)2.
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
5.下列离子或分子组在溶液中能大量共存的是( )
| A. | K+ NO3- I- H2SO3 | B. | Na+ Fe3+ NO3- SCN- | ||
| C. | K+ AlO2- CO32- Al3+ | D. | NH4+ Mg2+ SO42- CH3COOH |
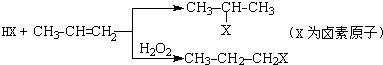
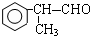 的物质,该物质是一种香料.
的物质,该物质是一种香料.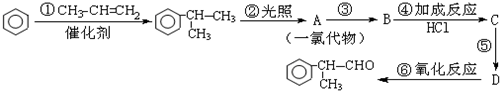
 、
、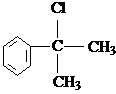 +NaOH$→_{△}^{乙醇}$
+NaOH$→_{△}^{乙醇}$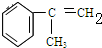 +NaCl+H2O.
+NaCl+H2O. +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2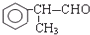 +2H2O.
+2H2O.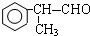 有多种同分异构体,满足下列条件:(1)苯环上一卤代物有两种,(2)属于醛类的同分异构体有4种.
有多种同分异构体,满足下列条件:(1)苯环上一卤代物有两种,(2)属于醛类的同分异构体有4种.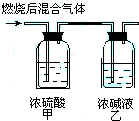 燃烧法是测定有机化合物化学式的一种重要方法.现在完全燃烧0.1mol某烃,燃烧产物依次通过如图所示的装置,实验结束后,称得甲装置增重10.8g,乙装置增重22g.求该烃的化学式.
燃烧法是测定有机化合物化学式的一种重要方法.现在完全燃烧0.1mol某烃,燃烧产物依次通过如图所示的装置,实验结束后,称得甲装置增重10.8g,乙装置增重22g.求该烃的化学式. 则:
则: