题目内容
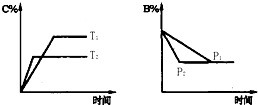 可逆反应aA(s)+bB(g)?cC(g)+dD(g),△H=Q,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图示据图分析,以下正确的是( )
可逆反应aA(s)+bB(g)?cC(g)+dD(g),△H=Q,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图示据图分析,以下正确的是( )| A、T1>T2,Q>0 |
| B、Tl<T2,Q<0 |
| C、P1>P2,a+b=c+d |
| D、Pl<P2,b=c+d |
考点:体积百分含量随温度、压强变化曲线
专题:化学平衡专题
分析:根据“先拐先平数值大”确定温度、压强的大小关系,再根据温度、压强的改变对物质百分含量的改变确定其反应热、气体计量数之间的关系,据此分析解答.
解答:
解:根据“先拐先平数值大”知,Tl<T2、Pl<P2,当升高温度时,C的百分含量减小,说明平衡向逆反应方向移动,则正反应是放热反应,Q<0;当增大压强时,B的百分含量不变,说明压强对该反应无影响,则反应前后气体的计量数之和不变,即b=c+d,故选BD.
点评:本题考查了温度、压强对化学平衡的影响图象分析,明确“先拐先平数值大”是解本题关键,根据外界条件改变对反应的影响确定反应热、气体的计量数变化,题目难度不大.

练习册系列答案
相关题目
有8种物质:①乙烷;②乙烯;③聚1,3-丁二烯;④苯;⑤2-丁炔;⑥溴乙烷;⑦聚丙烯;⑧环己烯;⑨邻二甲苯.其中既不能使酸性KMnO4溶液褪色,也不能与溴水反应使溴水褪色的是( )
| A、①③⑤⑦ | B、①③④⑧ |
| C、①④⑥⑦ | D、②③⑤⑧ |
聚合物 的单体是( )
的单体是( )
 的单体是( )
的单体是( )A、 |
| B、CH2=CH2 |
C、 |
D、 |
下列关于1.0L 0.1mol/L的盐酸溶液的说法正确的是( )
| A、该溶液中含6.02×1022个HCl分子 |
| B、标准状况下2.24L HCl溶于1L水中所得的溶液 |
| C、将500mL 0.2mol/L的盐酸加水稀释到1L所得的溶液 |
| D、将2.0L 0.05mol/L的盐酸蒸发浓缩到体积为1L所得的溶液 |
下列实验装置图中没有涉及气体压强原理的是( )
A、 |
B、 |
C、 |
D、 |
下列各组物质混合后,再加热蒸干并在300℃时充分灼烧至质量不变,最终一定能得到纯净物的是( )
| A、向FeSO4溶液中通入过量Cl2 |
| B、向NaHCO3溶液中加入一定质量的Na2O2粉末 |
| C、向NaI和NaBr混合溶液中通入过量Cl2 |
| D、向NaOH溶液中加入过量AlCl3 |
X、Y、Z、W、M 均为短周期元素,X、Y 同主族,X 的氢化物和最高价氧化物的水化物能反应生成一种离子化合物;Z、W、M 是第3 周期连续的三种元素,其中只有一种是非金属,且原子半径Z>W>M.下列叙述准确的是( )
| A、X、M 两元素氢化物的稳定性:X<M |
| B、X、Y、M 的单质的氧化性:X>Y>M |
| C、Z、W单质均易与冷水反应 |
| D、Z、W、M 的单质均能与NaOH溶液反应制取氢气 |
在同温、同压下,有同质量的气体X和Y.已知此时Y的体积大于X的体积,则它们的相对分子质量关系是( )
| A、MX>MY |
| B、MX<MY |
| C、MX=MY |
| D、无法确定 |
下面的排序不正确的是( )
| A、晶体熔点由低到高:CH4<SiH4<GeH4<SnH4 |
| B、熔点由高到低:Rb>K>Na |
| C、硬度由大到小:金刚石>碳化硅>晶体硅 |
| D、晶格能由大到小:NaF>NaCl>NaBr>NaI |