题目内容
X、Y、Z、W、M 均为短周期元素,X、Y 同主族,X 的氢化物和最高价氧化物的水化物能反应生成一种离子化合物;Z、W、M 是第3 周期连续的三种元素,其中只有一种是非金属,且原子半径Z>W>M.下列叙述准确的是( )
| A、X、M 两元素氢化物的稳定性:X<M |
| B、X、Y、M 的单质的氧化性:X>Y>M |
| C、Z、W单质均易与冷水反应 |
| D、Z、W、M 的单质均能与NaOH溶液反应制取氢气 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W、M 均为短周期元素,X 的氢化物和最高价氧化物的水化物能反应生成一种离子化合物,应为铵盐,则X为N元素;X、Y 同主族,则Y为P;Z、W、M 是第3 周期连续的三种元素,其中只有一种是非金属,且原子半径Z>W>M,可推知Z为Mg、W为Al、M为Si,结合元素周期律与元素化合物性质解答.
解答:
解:X、Y、Z、W、M 均为短周期元素,X 的氢化物和最高价氧化物的水化物能反应生成一种离子化合物,应为铵盐,则X为N元素;X、Y 同主族,则Y为P;Z、W、M 是第3 周期连续的三种元素,其中只有一种是非金属,且原子半径Z>W>M,可推知Z为Mg、W为Al、M为Si,
A.非金属性X(N)>M(Si),故两元素氢化物的稳定性:X>M,故A错误;
B.非金属性X(N)>Y(P)>M(Si),故单质的氧化性:X>Y>M,故B正确;
C.Mg与冷水发生微弱反应,而Al与冷水不反应,故C错误;
D.Mg与氢氧化钠溶液不反应,故D错误,
故选B.
A.非金属性X(N)>M(Si),故两元素氢化物的稳定性:X>M,故A错误;
B.非金属性X(N)>Y(P)>M(Si),故单质的氧化性:X>Y>M,故B正确;
C.Mg与冷水发生微弱反应,而Al与冷水不反应,故C错误;
D.Mg与氢氧化钠溶液不反应,故D错误,
故选B.
点评:本题考查结构性质位置关系应用,推断元素是解题关键,注意掌握元素化合物知识,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在25℃时,将amol/L的氨水和0.01mol/L的盐酸溶液等体积混合,反应溶液呈中性,下列说法错误的是(忽略溶液混合体积的变化)( )
| A、溶液中有c(NH4+)=c(Cl-) | ||
| B、此时水的电离程度最大 | ||
C、此时溶液中氨水的物质的量浓度为
| ||
| D、a>0.01 |
下列说法正确的是( )
| A、因为SO2具有漂白性,所以它能使品红溶液、溴水、酸性KMnO4溶液、石蕊试液褪色 |
| B、能使品红溶液褪色的物质不一定是SO2 |
| C、SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,且原理相同 |
| D、等物质的量的SO2和Cl2混合后通入装有湿润的有色布条的集气瓶中,漂白效果更好 |
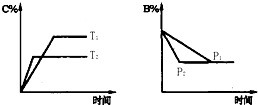 可逆反应aA(s)+bB(g)?cC(g)+dD(g),△H=Q,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图示据图分析,以下正确的是( )
可逆反应aA(s)+bB(g)?cC(g)+dD(g),△H=Q,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图示据图分析,以下正确的是( )| A、T1>T2,Q>0 |
| B、Tl<T2,Q<0 |
| C、P1>P2,a+b=c+d |
| D、Pl<P2,b=c+d |
实验室从碘水中得到纯净的碘的操作,正确的是( )
| A、分液、蒸馏 |
| B、过滤、蒸发 |
| C、萃取、分液 |
| D、萃取、分液、蒸馏 |
下列离子方程式中正确的是( )
| A、FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | ||
| B、等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3?H2O+H2O | ||
C、碳酸氢镁溶液中加入过量石灰水 Mg2++2HCO
| ||
| D、硫化钠溶于水中:S2-+2H2O=H2S↑+2OH- |
m mol H2SO4中含有n个氧原子,则阿伏加德罗常数可以表示为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列说法中正确的是( )
| A、乙烯和苯都能使溴水褪色,褪色的原因相同 |
| B、开发核能、太阳能等新能源,推广基础甲醇汽油,使用无磷洗涤剂都可直接降低碳排放 |
| C、光导纤维、棉花、油脂、ABS树脂都是由高分子化合物组成的物质 |
| D、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 |
一定条件下,反应N2+3H2=2NH3在2L密闭容器中进行,5min内氨的质量增加1.7g,则在这段时间内的反应速率是( )
| A、v(NH3)=0.17g?L-1?s-1 |
| B、v(NH3)=0.02mol?L-1?min-1 |
| C、v(N2)=0.01mol?L-1?min-1 |
| D、v(H2)=0.015mol?L-1?min-1 |