题目内容
下列关于1.0L 0.1mol/L的盐酸溶液的说法正确的是( )
| A、该溶液中含6.02×1022个HCl分子 |
| B、标准状况下2.24L HCl溶于1L水中所得的溶液 |
| C、将500mL 0.2mol/L的盐酸加水稀释到1L所得的溶液 |
| D、将2.0L 0.05mol/L的盐酸蒸发浓缩到体积为1L所得的溶液 |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:A.HCl分子溶于水完全电离;
B.溶液的体积不等于溶剂的体积;
C.溶液稀释前后溶质的物质的量不变;
D.盐酸蒸发,溶质挥发.
B.溶液的体积不等于溶剂的体积;
C.溶液稀释前后溶质的物质的量不变;
D.盐酸蒸发,溶质挥发.
解答:
解:A.HCl分子溶于水完全电离,溶液中不含有HCl分子,故A错误;
B.标准状况下2.24L HCl溶于1L水中,所得的溶液的体积不是1L,故B错误;
C.将500mL 0.2mol/L的盐酸加水稀释到1L所得的溶液,溶液稀释前后溶质的物质的量不变,则有:500mL×0.2mol/L=1000mL×C,解得:C=0.1mol/L,故C正确;
D.将2.0L 0.05mol/L的盐酸蒸发浓缩到体积为1L所得的溶液,溶质挥发,无法计算溶质的物质的量,故D错误;
故选C.
B.标准状况下2.24L HCl溶于1L水中,所得的溶液的体积不是1L,故B错误;
C.将500mL 0.2mol/L的盐酸加水稀释到1L所得的溶液,溶液稀释前后溶质的物质的量不变,则有:500mL×0.2mol/L=1000mL×C,解得:C=0.1mol/L,故C正确;
D.将2.0L 0.05mol/L的盐酸蒸发浓缩到体积为1L所得的溶液,溶质挥发,无法计算溶质的物质的量,故D错误;
故选C.
点评:本题考查物质的量浓度的理解与计算,难度较小,注意物质的量浓度中体积指溶液体积,物质溶于水溶质变化的情况.

练习册系列答案
相关题目
下列说法或表示法正确的是( )
| A、等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、由C(石墨)→C(金刚石)△H=+119kJ?mol-1可知,石墨比金刚石稳定 |
| C、在稀溶液中:H++OH-═H2O△H=-57.3kJ?mol-1,若将含1molCH3COOH的醋酸溶液与含1molNaOH的溶液混合,放出的热量等于57.3kJ |
| D、在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l)△H=+285.8 kJ?mol-1 |
下列离子方程式正确的是( )
| A、铜与硝酸银溶液反应:Cu+Ag+=Cu2++Ag |
| B、硫酸与氢氧化钡溶液反应:OH-+Ba2++SO42-+H+=BaSO4↓+H2O |
| C、碳酸钙和盐酸反应:CO32-+2H+=CO2↑+H2O |
| D、硫酸铜与氢氧化钡溶液反应:Cu2++SO42-+Ba2++2OH-=BaSO4↓+Cu(OH)2↓ |
下列所述变化规律正确的是( )
| A、Na、Mg、Al还原性依次增强 |
| B、HCl、PH3、H2S稳定性依次减弱 |
| C、NaOH、KOH、CsOH碱性依次增强 |
| D、S2-、Cl-、K+、Ca2+离子半径依次增大 |
下列说法正确的是( )
| A、因为SO2具有漂白性,所以它能使品红溶液、溴水、酸性KMnO4溶液、石蕊试液褪色 |
| B、能使品红溶液褪色的物质不一定是SO2 |
| C、SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,且原理相同 |
| D、等物质的量的SO2和Cl2混合后通入装有湿润的有色布条的集气瓶中,漂白效果更好 |
下列各组物质中,互为同素异形体的是( )
| A、T2O与D2O | ||||
B、
| ||||
| C、O2和O3 | ||||
D、
|
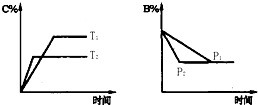 可逆反应aA(s)+bB(g)?cC(g)+dD(g),△H=Q,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图示据图分析,以下正确的是( )
可逆反应aA(s)+bB(g)?cC(g)+dD(g),△H=Q,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图示据图分析,以下正确的是( )| A、T1>T2,Q>0 |
| B、Tl<T2,Q<0 |
| C、P1>P2,a+b=c+d |
| D、Pl<P2,b=c+d |
下列离子方程式中正确的是( )
| A、FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | ||
| B、等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3?H2O+H2O | ||
C、碳酸氢镁溶液中加入过量石灰水 Mg2++2HCO
| ||
| D、硫化钠溶于水中:S2-+2H2O=H2S↑+2OH- |
白磷和红磷可以相互转化,它们在氧气中燃烧后都生成五氧化二磷,这一事实说明了白磷和红磷互为( )
| A、同一单质 | B、同位素 |
| C、同素异形体 | D、同分异构体 |