题目内容
 将Mg和Al粉末均匀混合,加入到100mL某浓度的硫酸中,产生氢气的体积(标准状况下)与加入粉末的质量关系如图所示:
将Mg和Al粉末均匀混合,加入到100mL某浓度的硫酸中,产生氢气的体积(标准状况下)与加入粉末的质量关系如图所示:(1)硫酸物质的量浓度是
(2)当硫酸溶液为350mL,固体粉末为33.3g时,充分反应后产生的气体体积为
(3)原固体混合物中Mg和Al的物质的量之比为
考点:有关混合物反应的计算
专题:计算题
分析:(1)加入Mg、Al混合物11.1g时,硫酸完全反应,根据氢气的体积计算硫酸的物质的量,进而计算硫酸的物质的量浓度;
若向反应后的滤液中滴加5mol?L-1氢氧化钠溶液,当得到最大沉淀时,镁离子、铝离子转化为氢氧化镁、氢氧化铝沉淀,产生溶液中溶质为Na2SO4,由硫酸根守恒n(Na2SO4)=n(H2SO4),由钠离子守恒可知n(NaOH)=2n(Na2SO4),再根据V=
计算;
(2)100mL硫酸完全反应需要混合物质量11.1g,生成氢气为11.2L,故350mL硫酸完全反应需要混合物的质量=11.1g×
=38.85g>33.3g,故硫酸有剩余,根据混合物的质量计算生成氢气的体积;
(3)令11.1g混合物中Mg、Al的物质的量分别为x mol、y mol,根据二者质量及电子转移守恒列方程计算.
若向反应后的滤液中滴加5mol?L-1氢氧化钠溶液,当得到最大沉淀时,镁离子、铝离子转化为氢氧化镁、氢氧化铝沉淀,产生溶液中溶质为Na2SO4,由硫酸根守恒n(Na2SO4)=n(H2SO4),由钠离子守恒可知n(NaOH)=2n(Na2SO4),再根据V=
| n |
| c |
(2)100mL硫酸完全反应需要混合物质量11.1g,生成氢气为11.2L,故350mL硫酸完全反应需要混合物的质量=11.1g×
| 350mL |
| 100mL |
(3)令11.1g混合物中Mg、Al的物质的量分别为x mol、y mol,根据二者质量及电子转移守恒列方程计算.
解答:
解:(1)加入Mg、Al混合物11.1g时,硫酸完全反应,生成氢气11.2L,氢气的物质的量=
=0.5mol,由H2SO4~H2可知n(H2SO4)=n(H2)=0.5mol,故c(H2SO4)=
=5mol/L;
若向反应后的滤液中滴加5mol?L-1氢氧化钠溶液,当得到最大沉淀时,镁离子、铝离子转化为氢氧化镁、氢氧化铝沉淀,产生溶液中溶质为Na2SO4,由硫酸根守恒n(Na2SO4)=n(H2SO4)=0.5mol,由钠离子守恒可知n(NaOH)=2n(Na2SO4)=1mol,故需要氢氧化钠溶液的体积=
=0.2L=200mL,
故答案为:5;200;
(2)100mL硫酸完全反应需要混合物质量11.1g,生成氢气为11.2L,故350mL硫酸完全反应需要混合物的质量=11.1g×
=38.85g>33.3g,故硫酸有剩余,33.3g混合物完全反应,故生成氢气的体积=11.2L×
=33.6L,
故答案为:33.6;
(3)令11.1g混合物中Mg、Al的物质的量分别为x mol、y mol,根据二者质量及电子转移守恒列方程,则:
解得x=0.35、y=0.1,
故原固体混合物中Mg和Al的物质的量之比为0.35mol:0.1mol=7:2
故答案为:7:2.
| 11.2L |
| 22.4L/mol |
| 0.5mol |
| 0.1L |
若向反应后的滤液中滴加5mol?L-1氢氧化钠溶液,当得到最大沉淀时,镁离子、铝离子转化为氢氧化镁、氢氧化铝沉淀,产生溶液中溶质为Na2SO4,由硫酸根守恒n(Na2SO4)=n(H2SO4)=0.5mol,由钠离子守恒可知n(NaOH)=2n(Na2SO4)=1mol,故需要氢氧化钠溶液的体积=
| 1mol |
| 5mol/L |
故答案为:5;200;
(2)100mL硫酸完全反应需要混合物质量11.1g,生成氢气为11.2L,故350mL硫酸完全反应需要混合物的质量=11.1g×
| 350mL |
| 100mL |
| 33.3g |
| 11.1g |
故答案为:33.6;
(3)令11.1g混合物中Mg、Al的物质的量分别为x mol、y mol,根据二者质量及电子转移守恒列方程,则:
|
解得x=0.35、y=0.1,
故原固体混合物中Mg和Al的物质的量之比为0.35mol:0.1mol=7:2
故答案为:7:2.
点评:本题考查混合物计算、化学反应图象有关计算,侧重考查学生获取信息的能力、分析解决问题的能力,注意守恒思想运用,难度中等.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案
相关题目
已知氧化性:Br2>Fe3+>I2,向含有a mol FeI2的溶液中加入含b mol Br2的溴水,下列判断或相应的离子方程式正确的是( )
| A、当a=2,b=1时,离子方程式为:2Fe2++Br2→2Fe3++2Br- | ||||
B、如果反应后的溶液中存在c(Fe2+)=c(Fe3+),则
| ||||
| C、当a=1,b=2时,离子方程式为:2Fe2++4I-+3Br2→2Fe3++2I2+6Br- | ||||
| D、当a=2,2<b<3时,溶液中铁元素以两种离子形式存在,且一定是c(Fe3+)>c(Fe2+) |
 19世纪丹麦学者尤利乌斯?托姆森得到一个计算CuCl2?2H2O在水中溶解热效应(设为△H,且当△H<0,放热;△H>0吸热)的式子,当所得溶液中1mol CuCl2有x mol水时,所产生的热效应△H=[3.35-21.02×
19世纪丹麦学者尤利乌斯?托姆森得到一个计算CuCl2?2H2O在水中溶解热效应(设为△H,且当△H<0,放热;△H>0吸热)的式子,当所得溶液中1mol CuCl2有x mol水时,所产生的热效应△H=[3.35-21.02×| (x-10) |
| x+11.24 |
| A、仅根据题中信息,无法计算出20℃时CuCl2饱和溶液的物质的量浓度 |
| B、当x<10,因CuCl2不能完全溶解,上图无物理意义 |
| C、在极稀的溶液中,1 mol CuCl2溶液时约放出17.67kJ热量 |
| D、CuCl2?2H2O溶于水是放热的 |
 工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤.
工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤. 利用氮气、氢气在一定条件下生成氨气这一可逆反应来合成氨,是一个重要的化工反应.常用来生产液氨和氨水.完成下列填空:
利用氮气、氢气在一定条件下生成氨气这一可逆反应来合成氨,是一个重要的化工反应.常用来生产液氨和氨水.完成下列填空: 有如下化学反应:2A(g)+B(g)??2C(g)(正反应为放热反应).
有如下化学反应:2A(g)+B(g)??2C(g)(正反应为放热反应).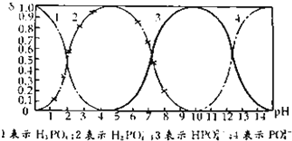 磷酸(H3PO4)在溶液中能够以H3PO4、H2PO4-、HPO42-和PO43-四种粒子的形式存在,当溶液中的pH发生变化时,其中任一种粒子的物质的量占四种粒子总物质的量的分数δ也可能发生变化.如图所示是H3PO4溶液中,各种粒子的物质的量分数δ随pH变化曲线:
磷酸(H3PO4)在溶液中能够以H3PO4、H2PO4-、HPO42-和PO43-四种粒子的形式存在,当溶液中的pH发生变化时,其中任一种粒子的物质的量占四种粒子总物质的量的分数δ也可能发生变化.如图所示是H3PO4溶液中,各种粒子的物质的量分数δ随pH变化曲线: