题目内容
 19世纪丹麦学者尤利乌斯?托姆森得到一个计算CuCl2?2H2O在水中溶解热效应(设为△H,且当△H<0,放热;△H>0吸热)的式子,当所得溶液中1mol CuCl2有x mol水时,所产生的热效应△H=[3.35-21.02×
19世纪丹麦学者尤利乌斯?托姆森得到一个计算CuCl2?2H2O在水中溶解热效应(设为△H,且当△H<0,放热;△H>0吸热)的式子,当所得溶液中1mol CuCl2有x mol水时,所产生的热效应△H=[3.35-21.02×| (x-10) |
| x+11.24 |
| A、仅根据题中信息,无法计算出20℃时CuCl2饱和溶液的物质的量浓度 |
| B、当x<10,因CuCl2不能完全溶解,上图无物理意义 |
| C、在极稀的溶液中,1 mol CuCl2溶液时约放出17.67kJ热量 |
| D、CuCl2?2H2O溶于水是放热的 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、c=
,不知道密度,无法计算V;
B、据20℃时的溶解度可以算出,1molCuCl2溶解,至少需要水的物质的量可得;
C、极稀的溶液,x无限大;
D、从图象分析,x<15时,△H>0;
| n |
| V |
B、据20℃时的溶解度可以算出,1molCuCl2溶解,至少需要水的物质的量可得;
C、极稀的溶液,x无限大;
D、从图象分析,x<15时,△H>0;
解答:
解:A、不知道溶液的密度,无法计算溶液的体积,所以,无法求得溶液的物质的量浓度,故A正确;
B、1molCuCl2溶解,在20℃时达到饱和,需要水的量超过10mol,所以x<10时,上图无意义,故B正确;
C、极稀的溶液,可以认为x无限大,
近似与1,则△H=[3.35-21.02×
]kJ?mol-1=[3.35-21.02]kJ?mol-1=-17.67KJ/mol,故C正确;
D、从图象分析,x<15时,△H>0吸热,故D错误;
故选:D.
B、1molCuCl2溶解,在20℃时达到饱和,需要水的量超过10mol,所以x<10时,上图无意义,故B正确;
C、极稀的溶液,可以认为x无限大,
| x-10 |
| x+11.24 |
| (x-10) |
| x+11.24 |
D、从图象分析,x<15时,△H>0吸热,故D错误;
故选:D.
点评:本题是信息给予题,考查学生的自学能力、识图能力、以及物质的量浓度的计算的相关知识,题目难度中等.

练习册系列答案
相关题目
如图是两个氢原子相互接近时的能量变化图,则有关该图的说法正确的是( )
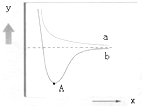

| A、y代表两原子之间的核间距 |
| B、x代表体系具有的能量 |
| C、a代表核外电子自旋相反的两个氢原子能量变化 |
| D、A点时表示两原子间形成了稳定的共价键 |
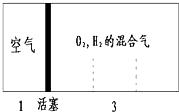 如图所示装置,室温下密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积比最接近于( )
如图所示装置,室温下密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则原来H2、O2的体积比最接近于( )①2:7 ②5:4 ③4:5 ④7:2.
| A、①② | B、③④ | C、②④ | D、①③ |
X、Y、Z、W为四种短周期非金属元素,其中X单质是一种重要的半导体材料,X、Y、Z同周期,且原子序数依次增大,Y、W同主族,离子半径Y2->W2-.下列说法正确的是( )
| A、X的非金属性比Y的强 |
| B、X和W组成的化合物化学性质活泼,与盐酸和氢氧化钠溶液都能反应 |
| C、Y的气态氢化物不如Z的气态氢化物稳定 |
| D、某溶液中通入Z的单质,再滴加淀粉溶液显蓝色,原溶液中一定含有I- |
若阿伏加德罗常数的值为6.02×1023,则下列叙述正确的是( )
| A、标准状况下,2.24L戊烷中含有2.408×1023个碳碳单键 |
| B、100mL 1mol/L 的Na2CO3溶液中含有6.02×1022个CO32- |
| C、1mol氨气与1mol NH4+中所电子数均为6.02×1024 |
| D、将3.9g Na2O2放入足量的水中,反应时转移6.02×1022个电子 |
下列有关实验说法中,错误的是( )
| A、葡萄糖银镜反应实验后的试管内壁附有银,可用氨水清洗 |
| B、酸碱中和滴定时,未用待测液润洗锥形瓶,对测定结果无影响 |
| C、向某溶液中加入足量盐酸无现象,再加入BaCl2溶液生成白色沉淀说明有SO42- |
| D、在无色溶液中先加入氯水、再加入CCl4,振荡静置,下层溶液显红棕色说明有Br- |
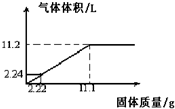 将Mg和Al粉末均匀混合,加入到100mL某浓度的硫酸中,产生氢气的体积(标准状况下)与加入粉末的质量关系如图所示:
将Mg和Al粉末均匀混合,加入到100mL某浓度的硫酸中,产生氢气的体积(标准状况下)与加入粉末的质量关系如图所示: