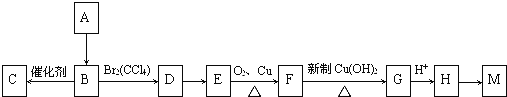
题目内容
【题目】25℃时,某溶液中由水电离出的c(OH-)=1×10-13mol/L,该溶液中一定不能大量共存的离子组是( )
A.NH![]() 、Fe3+、SO
、Fe3+、SO![]() 、Cl-B.CO
、Cl-B.CO![]() 、PO
、PO![]() 、K+、Na+
、K+、Na+
C.Na+、SO![]() 、NO
、NO![]() 、Cl-D.HPO
、Cl-D.HPO![]() 、Na+、HSO
、Na+、HSO![]() 、K+
、K+
【答案】D
【解析】
25℃时某溶液中由水电离出c(OH-)=1×10-13mol/L的溶液呈酸性或碱性;
A.NH4+、Fe3+、SO42-、Cl-之间不反应,都不与H+反应,在酸性溶液中能够大量共存,故A不符合题意;
B.CO32-、PO43-、K+、Na+之间不反应,都不与OH-反应,在碱性溶液中能够大量共存,故B不符合题意;
C.Na+、SO42-、NO3-、Cl-之间不反应,都不与H+和OH-反应,在酸性或碱性溶液中都能够大量共存,故C不符合题意;
D.HPO![]() 、HSO
、HSO![]() 与H+和OH-都反应,在酸性或碱性溶液中一定不能大量共存,故D符合题意;
与H+和OH-都反应,在酸性或碱性溶液中一定不能大量共存,故D符合题意;
故答案为D。

【题目】一定温度下,在三个体积均为0.5 L的恒容密闭容器中发生反应:CO(g)+Cl2(g) ![]() COCl2(g),其中容器Ⅰ中反应在5 min时达到平衡状态。
COCl2(g),其中容器Ⅰ中反应在5 min时达到平衡状态。
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
CO | Cl2 | COCl2 | COCl2 | ||
Ⅰ | 500 | 1.0 | 1.0 | 0 | 0.8 |
Ⅱ | 500 | 1.0 | a | 0 | 0.5 |
Ⅲ | 600 | 0.5 | 0.5 | 0.5 | 0.7 |
下列说法中正确的是
A.该反应正反应为放热反应
B.容器Ⅰ中前5 min的平均反应速率υ(CO)=0.16 mol·L-1·min-1
C.容器Ⅱ中,a=0.55 mol
D.若容器Ⅰ为恒压,达到平衡时CO转化率小于80%
【题目】请根据要求填写下列空白:
(1)NaHCO3溶液呈碱性的原因是 ______________(用方程式和必要文字表示),写出该溶液存在的物料守恒的关系式 ________________。
(2)把AlCl3溶液蒸干、灼烧,最后得到的主要产物是________________________。
(3)若想除去CuCl2 溶液中混有FeCl3杂质,则往往加入试剂 ______________。
①NaOH ②NH3·H2O ③CuO ④CuCO3
(4)在酸碱滴定中,我们用0.1000mol/L HCl来滴定未知浓度的NaOH溶液,①在滴定过程中,操作或说法错误的是_______________。
a.滴定终点为:当滴完最后一滴恰好变色,且在半分钟内不恢复原色
b.进行中和滴定操作时,左手震荡锥形瓶,右手转动活塞控制液滴流速,眼睛要始终注视滴定管内溶液液面的变化
c.酸式滴定管中的盐酸装液前未经润洗,导致所测定的c(NaOH)偏低。
d.酸式滴定管在滴定前有气泡,滴定后气泡消失,导致所测定的c(NaOH)偏高
②某学生根据三次实验分别记录有关数据如下:
滴定次数 | 待测氢氧化钠 溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | ||
滴定前刻度 | 滴定后刻度 | 溶液体/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
请选用其中合理的数据列式计算该氢氧化钠溶液的物质的量浓度:c(NaOH)=________________