题目内容
 某温度时,在一个容积为2L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:
某温度时,在一个容积为2L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,试填写下列空白:(1)该反应的化学方程式为
(2)反应开始至2min,用气体Z表示的反应速率为
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的
②若此时将容器的体积缩小为原来的0.5倍,达到平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应的正反应为
考点:化学平衡的计算
专题:化学平衡专题
分析:(1)根据物质的量变化曲线,可知X、Y物质的量减小,为反应物;反应物没有完全反应,所以该反应为可逆反应;Z物质的量增加,为生成物,再根据其物质的量变化量之比等于其计量数之比,可写出化学方程式;
(2)根据2min内Z物质的量变化量和容器体积,可知道浓度变化量,通过计算可知用气体Z表示的反应速率;
(3)①气体的压强之比等于气体的物质的量之比,可求出开始时气体的总物质的量和平衡后气体总物质的量,得到答案;
②体积缩小到原来的0.5倍,则压强变为原来的2倍,平衡向着气体体积缩小的方向移动,根据反应方程式可知,平衡向右移动;体系温度降低,说明平衡向着吸热的方向移动,根据分析得出答案.
(2)根据2min内Z物质的量变化量和容器体积,可知道浓度变化量,通过计算可知用气体Z表示的反应速率;
(3)①气体的压强之比等于气体的物质的量之比,可求出开始时气体的总物质的量和平衡后气体总物质的量,得到答案;
②体积缩小到原来的0.5倍,则压强变为原来的2倍,平衡向着气体体积缩小的方向移动,根据反应方程式可知,平衡向右移动;体系温度降低,说明平衡向着吸热的方向移动,根据分析得出答案.
解答:
解:(1)△n(X)=0.3mol;△n(Y)=0.1mol;△n(Z)=0.2mol,所以三者计量数之比为3:1:2,故答案为:3X+Y?2Z;
(2)v(Z)=
=
=
=0.05mol?L-1?min-1,故答案为:0.05mol?L-1?min-1;
(3)①根据图象中可知,开始时气体总物质的量为:2mol;平衡后气体总物质的量为:0.9mol+0.7mol+0.2mol=1.8mol;
=
=
=0.9,
故答案为:0.9;
②压强变大,平衡向右移动,而体系温度降低,说明正反应方向为吸热,故答案为:吸热.
(2)v(Z)=
| △c |
| △t |
| △n |
| V?△t |
| 0.2mol |
| 2L?2min |
(3)①根据图象中可知,开始时气体总物质的量为:2mol;平衡后气体总物质的量为:0.9mol+0.7mol+0.2mol=1.8mol;
| P平衡 |
| P起始 |
| n平衡 |
| n起始 |
| 1.8mol |
| 2mol |
故答案为:0.9;
②压强变大,平衡向右移动,而体系温度降低,说明正反应方向为吸热,故答案为:吸热.
点评:该题通过图象中物质的物质的量的变化,来考查化学平衡的移动、化学反应速率计算,还涉及到阿伏伽德罗定律,综合考查学生对知识的综合应用能力.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案
相关题目
下列方程式中,正确的是( )
| A、实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl-=Cl2↑+Mn2++H2O |
| B、氢氧化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| C、2mol氢气和1 mol氧气化合生成2 mol液态水,放出571.6kJ热量的热化学方程式2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ?mol-1 |
| D、醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
实验过程中不慎发生意外时,以下处理方法正确的是( )
| A、当有酸液溅入眼睛时,迅速揉搓 |
| B、苯酚溶液沾在皮肤上,立即用氢氧化钠溶液冲洗 |
| C、酸溶液流到实验桌上先用适量碳酸氢钠溶液冲洗,再用水冲洗 |
| D、酒精灯在桌面上倾倒后燃烧,立即用嘴吹灭 |
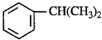
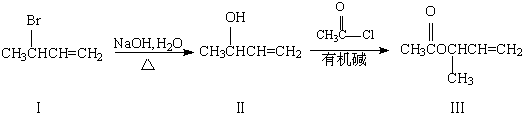
 ,俗名为水杨酸,在 医学上具有解热镇痛和抗炎、抗风湿作用,由于它具有酸性而刺激胃肠道产生严重的反应,因此通常将它先转化为乙酰水杨酸(阿司匹林),服用后在人体内会缓慢反应生成水杨酸:
,俗名为水杨酸,在 医学上具有解热镇痛和抗炎、抗风湿作用,由于它具有酸性而刺激胃肠道产生严重的反应,因此通常将它先转化为乙酰水杨酸(阿司匹林),服用后在人体内会缓慢反应生成水杨酸: