题目内容
16.下列说法中正确的是( )| A. | 煤燃烧是化学能转化为光能的过程 | |
| B. | 1 mol 甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 | |
| C. | HCl 和 NaOH 反应的中和热△H=-57.3 kJ•mol-1,则 H2SO4 和 Ca(OH)2 反应中和热△H=2×(-57.3)kJ•mol-1 | |
| D. | 反应 H2(g)+F2(g)═2HF(g);△H=-270 kJ•mol-1说明在相同条件下,1 mol 氢气与 1 mol 氟气的能量总和大于2 mol 氟化氢气体的能量 |
分析 A.煤燃烧发光放热;
B.燃烧热是1mol纯净的可燃物完全燃烧生成稳定氧化物放出的热量,水液态稳定;
C.中和热是强酸强碱的稀溶液完全反应生成1moil水放出的热量,硫酸钙微溶生成过程是放热过程;
D.反应 H2(g)+F2(g)═2HF(g);△H=-270 kJ•mol-1说明是放热反应,结合反应前后能量守恒分析判断.
解答 解:A.煤燃烧发光放热是化学能转化为光能、热能的过程,故A错误;
B.一定条件下,1 mol 甲烷燃烧生成液态水和二氧化碳所放出的热量是甲烷的燃烧热,气态水不稳定,故B错误;
C.HCl 和 NaOH 反应的中和热△H=-57.3 kJ•mol-1,则 H2SO4 和 Ca(OH)2 反应中硫酸钙微溶生成过程是放热,反应过程中和热△H<2×(-57.3)kJ•mol-1 ,故C错误;
D.反应 H2(g)+F2(g)═2HF(g),△H=-270 kJ•mol-1说明在相同条件下反应是放热反应,则依据反应前后能量守恒可知,1 mol 氢气与 1 mol 氟气的能量总和大于2 mol 氟化氢气体的能量,故D正确;
故选D.
点评 本题考查了化学反应能量变化、燃烧热和中和热概念实质理解,注意概念的应用条件,生成硫酸钙微溶,生成过程放热,题目难度中等.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
6.关于P、S、Cl三种元素的说法不正确的是( )
| A. | 原子半径 P>S>Cl | |
| B. | 最高价氧化物对应水化物的酸性 H3PO4<H2SO4<HClO4 | |
| C. | 氢化物的稳定性 PH3<H2S<HCl | |
| D. | 元素的非金属性 P>S>Cl |
7.原子序数依次递增的 4 种短周期元素可形成简单离子W2-、X+、Y3+、Z2-,下列说法不正确的是( )
| A. | 工业上常采用电解法冶炼Y 单质 | |
| B. | 气态氢化物的稳定性:H2W强于H2Z | |
| C. | 离子半径由大到小:Z2->X+>Y3+>W2- | |
| D. | W、X 形成的化合物中阴、阳离子个数比一定是1:2 |
1.下列各个反应,不能用于工业生产的是( )
| A. | 煅烧黄铁矿(FeS2)制SO2 | B. | 电解熔融氧化铝制金属铝 | ||
| C. | 钠与水反应制烧碱 | D. | 氯气与石灰乳反应制漂白粉 |
8.下列氯化物中,能由金属和盐酸直接制取,但不能由金属和氯气直接制取的是( )
| A. | AlCl3 | B. | FeCl2 | C. | FeCl3 | D. | CuCl2 |
5.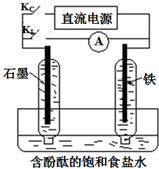 某研究性学习小组设计如下微型实验装置.实验时,先断开KL,闭合KC,两极均有气泡产生;一段时间后,断开KC,闭合KL,发现电流计A指针偏转.下列有关说法正确的是( )
某研究性学习小组设计如下微型实验装置.实验时,先断开KL,闭合KC,两极均有气泡产生;一段时间后,断开KC,闭合KL,发现电流计A指针偏转.下列有关说法正确的是( )
 某研究性学习小组设计如下微型实验装置.实验时,先断开KL,闭合KC,两极均有气泡产生;一段时间后,断开KC,闭合KL,发现电流计A指针偏转.下列有关说法正确的是( )
某研究性学习小组设计如下微型实验装置.实验时,先断开KL,闭合KC,两极均有气泡产生;一段时间后,断开KC,闭合KL,发现电流计A指针偏转.下列有关说法正确的是( )| A. | 断开KL,闭合KC时,铁作阴极,总反应方程式为2H2O=2H2↑+O2↑ | |
| B. | 断开KL,闭合KC时,石墨电极附近溶液变红 | |
| C. | 断开KC,闭合KL时,石墨作正极,发生还原反应Cl2+2e-=2Cl- | |
| D. | 断开KC,闭合KL时,铁作负极,发生铁的吸氧腐蚀反应 |



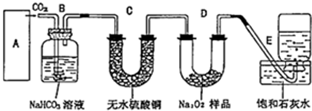 过氧化钠是一种淡黄色固体,在潜水艇中用作制氧剂,供人类呼吸之用.某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出实验装置(如图):
过氧化钠是一种淡黄色固体,在潜水艇中用作制氧剂,供人类呼吸之用.某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出实验装置(如图):