题目内容
元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法不正确的是( )
| A、第三周期元素从Na到Cl原子半径逐渐减小 |
| B、过渡元素全是金属元素,可用于寻找优良催化剂 |
| C、同一主族元素的单质,从上到下化学性质越来越活泼 |
| D、第三周期主族元素的最高正化合价数等于它所处的族序数 |
考点:元素周期表的结构及其应用,元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A.同周期,原子序数大的半径小;
B.在过渡元素区寻找优良的催化剂材料;
C.碱金属单质从上到下化学性质越来越活泼,而卤素单质从上到下化学性质越来越弱;
D.第三周期主族元素的最高正化合价数=最外层电子数.
B.在过渡元素区寻找优良的催化剂材料;
C.碱金属单质从上到下化学性质越来越活泼,而卤素单质从上到下化学性质越来越弱;
D.第三周期主族元素的最高正化合价数=最外层电子数.
解答:
解:A.同周期,原子序数大的半径小,则第三周期元素从Na到Cl原子半径逐渐减小,故A正确;
B.在过渡元素区寻找优良的催化剂材料,过渡元素含副族元素及第ⅤⅢ族元素,全是金属元素,故B正确;
C.碱金属单质从上到下化学性质越来越活泼,而卤素单质从上到下化学性质越来越弱,则同一主族元素的单质性质与金属性、非金属性有关,故C错误;
D.主族元素的原子结构中最外层电子数=等于它所处的族序数,第三周期主族元素的最高正化合价数=最外层电子数=等于它所处的族序数,故D正确;
故选C.
B.在过渡元素区寻找优良的催化剂材料,过渡元素含副族元素及第ⅤⅢ族元素,全是金属元素,故B正确;
C.碱金属单质从上到下化学性质越来越活泼,而卤素单质从上到下化学性质越来越弱,则同一主族元素的单质性质与金属性、非金属性有关,故C错误;
D.主族元素的原子结构中最外层电子数=等于它所处的族序数,第三周期主族元素的最高正化合价数=最外层电子数=等于它所处的族序数,故D正确;
故选C.
点评:本题考查周期表的结构及应用,为高频考点,把握元素的位置、性质、用途及元素周期律为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
氯气与碘在加热的条件下以一定比例反应可得的一红棕色液体ICl(氯化碘),ICl的性质类似于卤素,有很强的化学活动性.例如:ICl+H2O═HCl+HIO,2Zn+2ICl═ZnCl2+ZnI2,下列叙述正确的是( )
| A、在Zn跟ICl的反应中,ZnI2既是氧化产物又是还原产物 |
| B、在H2O跟ICl的反应中,ICl是氧化剂H2O是还原剂 |
| C、在Zn跟ICl的反应中,ZnCl2既是氧化产物又是还原产物 |
| D、在H2O跟ICl的反应中,ICl既是氧化剂又是还原剂 |
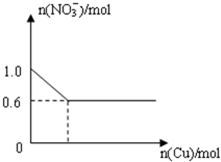 将28.8g铜投入100mL浓硝酸中,最后铜有剩余,其NO3-离子物质的量变化如图所示,请回答下列问题:
将28.8g铜投入100mL浓硝酸中,最后铜有剩余,其NO3-离子物质的量变化如图所示,请回答下列问题: