题目内容
下列反应的离子方程式书写正确的是( )
| A、氯气与NaOH溶液反应:Cl2+OH-=Cl-+ClO-+H2O |
| B、碳酸钙溶于醋酸溶液中:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、氧化镁与稀硫酸溶液反应:MgO+2H+=Mg2++H2O |
| D、钠与水反应:Na+H2O=Na++H2↑+OH- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.电荷不守恒,原子不守恒;
B.醋酸在离子反应中保留化学式;
C.反应生成硫酸镁和水;
D.电子不守恒.
B.醋酸在离子反应中保留化学式;
C.反应生成硫酸镁和水;
D.电子不守恒.
解答:
解:A.氯气与NaOH溶液反应的离子反应为Cl2+2OH-=Cl-+ClO-+H2O,故A错误;
B.碳酸钙溶于醋酸溶液中的离子反应为CaCO3+2HAc=Ca2++H2O+CO2↑+2Ac-,故B错误;
C.氧化镁与稀硫酸溶液反应的离子反应为MgO+2H+=Mg2++H2O,故C正确;
D.钠与水反应的离子反应为2Na+2H2O=2Na++H2↑+2OH-,故D错误;
故选C.
B.碳酸钙溶于醋酸溶液中的离子反应为CaCO3+2HAc=Ca2++H2O+CO2↑+2Ac-,故B错误;
C.氧化镁与稀硫酸溶液反应的离子反应为MgO+2H+=Mg2++H2O,故C正确;
D.钠与水反应的离子反应为2Na+2H2O=2Na++H2↑+2OH-,故D错误;
故选C.
点评:本题考查离子反应的书写,为高频考点,把握发生的化学反应及离子反应的书写方法为解答的关键,侧重复分解及氧化还原反应的离子反应考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列四种离子混合时不会发生反应的是( )
| A、OH-、Ca2+、CO32-、Cu2+ |
| B、Na+、Cl-、Mg2+、Fe3+ |
| C、H+、HCO3-、Al3+、CO32- |
| D、Ba2+、OH-、SO42-、NH4+ |
一定条件下进行反应:COCl2(g)?Cl2(g)+CO(g),向2.0L恒容密闭容器中充入1.0mol COCl2(g),经过一段时间后达到平衡.反应过程中测得的有关数据见下表:
下列说法正确的是( )
| t/s | 0 | 2 | 4 | 6 | 8 |
| n(Cl2)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
| A、保持其他条件不变,升高温度,平衡时c(Cl2)=0.22 mol?L-1,则反应的△H<0 |
| B、若在2 L恒容绝热(与外界没有热量交换)密闭容器进行该反应,化学平衡常数不变 |
| C、保持其他条件不变,起始向容器中充入1.2 molCOCl2、0.60 molCl2和0.60 molCO,反应达到平衡前的速率:v(正)<v(逆) |
| D、保持其他条件不变,起始向容器中充入1.0 molCl2和0.8 molCO,达到平衡时,Cl2的转化率小于60% |
PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物.2012年2月,国务院同意发布新修订的《环境空气质量标准》增加了PM2.5监测指标.下列情况不会增加空气中PM2.5的是( )
| A、露天焚烧秸秆 |
| B、直接用煤作燃料? |
| C、汽车排放尾气 |
| D、利用太阳能发电 |
铅蓄电池在现代生活中有广泛的应用.其反应原理如下:Pb+PbO2+4H++4SO42-
2PbSO4+2H2O下列说法正确的是( )
| 放电 |
| 充电 |
| A、电池放电时,负极失去电子,质量减轻 |
| B、电池放电时,电解质溶液中的H+向负极移动 |
| C、电池充电时,电池正极应和外接电源的正极相连接 |
| D、电池充电时,阴极反应为:Pb-2e-+SO42-=PbSO4 |
化学与社会、生活密切相关,下列说法中不正确的是( )
| A、区别地沟油(加工过的餐饮废弃油)和矿物油(汽油、煤油、柴油等)的方法是加入足量氢氧化钠溶液共热,不分层的是地沟油 |
| B、发泡塑料饭盒不适于盛放含油较多的食品 |
| C、光化学烟雾的产生与汽车排放的尾气有关 |
| D、将废电池深埋,可以避免其中的重金属污染 |

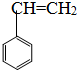 ;②CH3-CH=CH-CH3; ③CH2=CH-CH=CH2;④CH≡C-CH3;⑤
;②CH3-CH=CH-CH3; ③CH2=CH-CH=CH2;④CH≡C-CH3;⑤